Schmerzhafte diabetische Polyneuropathie: Eine Überarbeitung der Leitlinien ist erforderlich
Diabetic neuropathic pain: The guidelines should be revised
Zusammenfassung
Eine aktuelle Metaanalyse zur Pharmakotherapie der schmerzhaften diabetischen Polyneuropathie (1), die auch bisher unpublizierte Studien berücksichtigt, wird vorgestellt. Die Datenlage hinsichtlich der Wirksamkeit einzelner Wirkstoffe ist widersprüchlich. Eine Revision der Leitlinien erscheint erforderlich.
Abstract
A recent systematic review of the pharmacotherapy of diabetic neuropathic pain including unpublished studies is presented. The contradictory evaluation of some commonly prescribed drugs is discussed. The guidelines should be revised.
Einleitung
Etwa jeder zweite Diabetiker ist im Verlauf der Erkrankung von einer sensomotorischen Polyneuropathie betroffen (2). Häufig manifestiert sich die diabetische Polyneuropathie mit schmerzhaften, brennenden und kribbelnden Missempfindungen der Füße, die in späteren Stadien auch die Unterschenkel und Hände betreffen können. Schmerzen und Parästhesien können zu einer erheblichen Beeinträchtigung der Lebensqualität führen. In der klinischen Untersuchung zeigen sich neben einer reduzierten Wahrnehmung sensibler Reize (Minussymptomatik) gelegentlich auch Plussymptome mit mechanischer Allodynie (Schmerz nach leichter Berührung) sowie thermischer und mechanischer Hyperalgesie. Die Pathogenese der diabetischen Polyneuropathie ist unvollständig verstanden, als wesentliche Faktoren werden die Hyperglykämie und mikrovaskuläre Folgen des Diabetes mellitus diskutiert (3). Dass das Risiko der Entwicklung einer diabetischen Polyneuropathie durch eine normnahe Diabeteseinstellung reduziert werden kann, konnte zumindest für den Diabetes mellitus Typ 1 gezeigt werden (4). Für den Diabetes mellitus Typ 2 ist die Studienlage diesbezüglich dagegen uneinheitlich.
Prinzipien der Pharmakotherapie
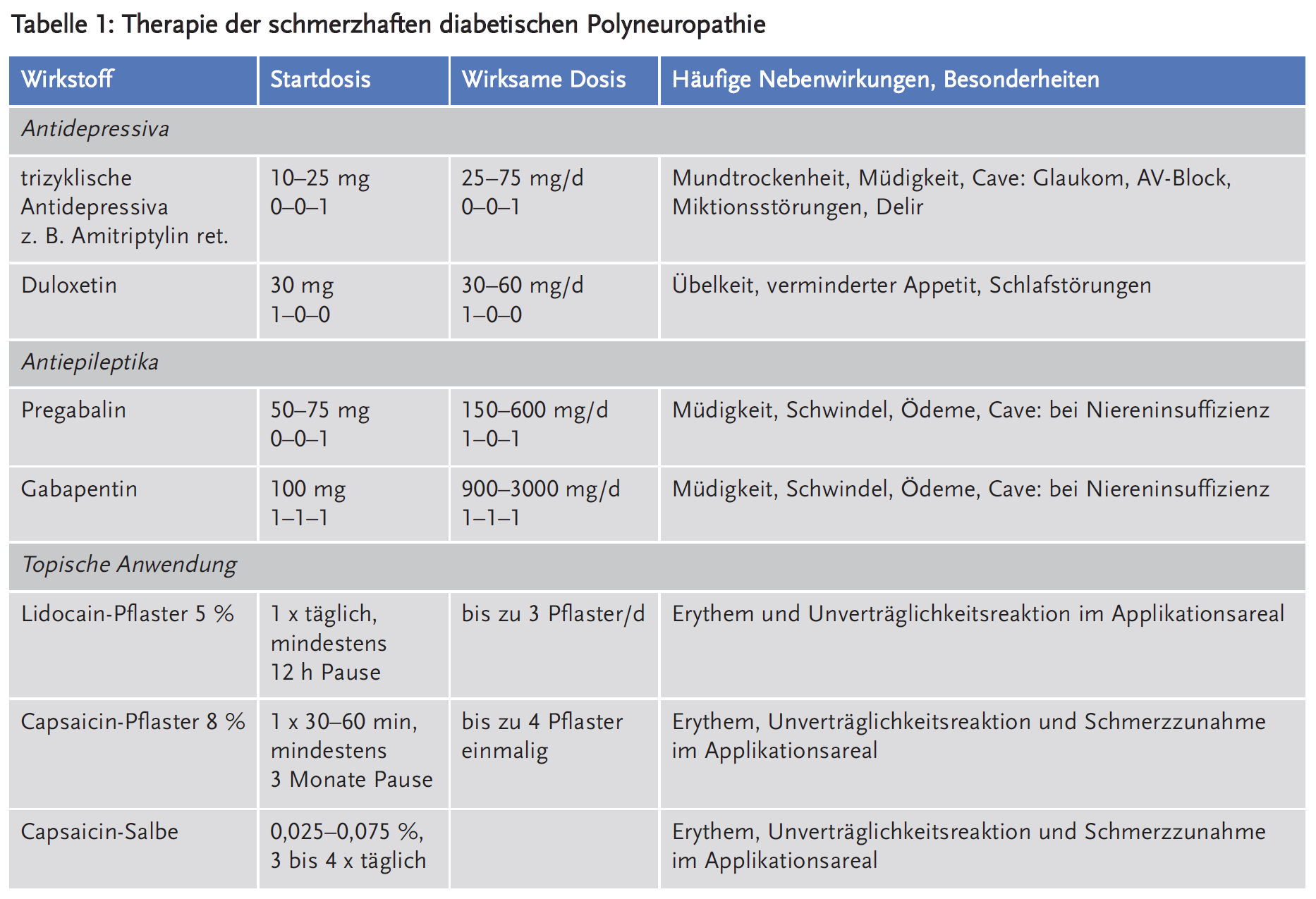
Zur Behandlung von neuropathischen Schmerzen infolge einer diabetischen Polyneuropathie werden vorwiegend Antidepressiva und Antiepileptika eingesetzt, seltener Opioide und topische Wirkstoffe (Tabelle 1). Beim individuellen Patienten muss die geeignete Therapie unter Berücksichtigung der Nebenwirkungen und Kontraindikationen erprobt werden. Alle oral eingenommenen Wirkstoffe müssen langsam aufdosiert werden, bis eine ausreichende Wirksamkeit erreicht ist oder unerwünschte Arzneimittelwirkungen den Einsatz begrenzen. Die erforderliche Dosis kann interindividuell stark differieren. Die Wirksamkeit sollte unter ausreichender Dosierung erst nach zwei bis vier Wochen beurteilt werden. Schmerzfreiheit wird selten erreicht. Der Patient sollte über eine Reduktion der Schmerzen um 30–50 % als realistisches Therapieziel informiert werden. Bei mangelnder Wirksamkeit oder unerwünschten Arzneimittelwirkungen ist ein Wechsel zu einer anderen Wirkstoffgruppe sinnvoll. Im Einzelfall kann die Kombination aus Wirkstoffen sinnvoll sein (5). Unerwünschte Arzneimittelwirkungen sind bei allen Wirkstoffen häufig und sind bei Antiepileptika und nicht-trizyklischen Antidepressiva vorwiegend Schwindel, Müdigkeit und Übelkeit, bei den trizyklischen Antidepressiva Mundtrockenheit und Müdigkeit.
Die Leitlinie der AWMF (zur Zeit in Überarbeitung) empfiehlt eine Therapie mit Pregabalin, Duloxetin und trizyklischen Antidepressiva (Empfehlungsgrad B) bzw. mit Opioiden (Empfehlungsgrad 0) (6). Für das in dieser Indikation häufig verordnete Gabapentin wurde die ursprüngliche Bewertung (Empfehlungsgrad 0) vorläufig außer Kraft gesetzt. Die Leitlinie der American Diabetes Association gibt Pregabalin und Duloxetin sogar den höchsten Empfehlungsgrad (7). Die Leitlinie der amerikanischen Neurologie-Fachgesellschaft bewertet ausschließlich Pregabalin mit dem Empfehlungsgrad A und bevorzugt diesen Wirkstoff somit vor allen anderen (8).
Neue Datenlage und Widersprüche
Eine aktuelle Metaanalyse zur Pharmakotherapie der schmerzhaften diabetischen Polyneuropathie (1) stellt die Empfehlungen der Leitlinien in Frage. Der systematische Review nahm die Ergebnisse einer 2014 publizierten Metaanalyse (9) als Grundlage und schloss zusätzlich 24 seither publizierte Studien und 25 unpublizierte Untersuchungen ein, die über die Website clinicaltrials.gov identifiziert wurden. Insgesamt wurden somit 106 Studien berücksichtigt. Einzig für die Serotonin-Noradrenalin-Wiederaufnahmehemmer Duloxetin und Venlafaxin wurde ein moderater Evidenzgrad ermittelt, für alle anderen Präparate war die Evidenz dagegen nur gering. Eine hohe Effektstärke wurde lediglich Venlafaxin bescheinigt, für Botulinumtoxin war sie moderat bis hoch. Diese beiden Wirkstoffe sind allerdings in Deutschland nicht in dieser Indikation zugelassenen. Eine moderate Effektstärke lag für Duloxetin, trizyklische Antidepressiva, atypische Opioide und Oxcarbazepin vor. Die Wirksamkeit von Pregabalin wurde dagegen als niedrig eingestuft. Als unwirksame Präparate wurden Gabapentin, typische Opioide und Capsaicin (0,075 %, topische Anwendung) eingestuft. Ein direkter Vergleich der Wirksamkeit dieser Präparate war aufgrund der Studienlage nicht möglich. Auch die Lebensqualität konnte mangels geeigneter Daten in dieser Metaanalyse nicht beurteilt werden. Zudem merkten die Autoren kritisch an, dass die Dauer der meisten Studien unter drei Monaten lag, obwohl in der Regel eine langfristige Therapie erforderlich ist.
Für Pregabalin liegen die mit Abstand meisten randomisierten und kontrollierten Studien zur Therapie der schmerzhaften diabetischen Polyneuropathie vor (16 Studien mit ca. 4000 Patienten). Allerdings ist bemerkenswert, dass Pregabalin in 7 von 10 neu identifizierten Studien in dieser Indikation keine Wirksamkeit gegenüber Placebo nachweisen konnte (1). Diese Beobachtung spricht für einen Publikationsbias, der zu den bisher hohen Empfehlungsgraden für Pregabalin in Leitlinien geführt haben dürfte.
Gabapentin ist ein weiterer, in dieser Indikation sehr häufig verordneter Wirkstoff, der als Kalziumkanalblocker einen ähnlichen Wirkmechanismus wie Pregabalin hat. Die AWMF-Leitlinie (6) hatte Gabapentin bisher mit dem niedrigsten Empfehlungsgrad bewertet. Aus nicht ersichtlichen Gründen kommen aktuelle Metaanalysen hinsichtlich der Wirksamkeit von Gabapentin bei der Therapie der schmerzhaften diabetischen Polyneuropathie zu sehr unterschiedlichen Ergebnissen. Eine Wirksamkeit wurde durch einen aktuellen Cochrane-Review ermittelt (NNT von 5,9 für eine Schmerzreduktion von mindestens 50 %) (10), nicht jedoch durch die Metaanalyse von Waldfogel und Mitarbeitern (1).
Bemerkenswert ist zudem, dass der besprochene Review suggeriert, dass Venlafaxin, das in Deutschland für die Therapie der schmerzhaften diabetischen Polyneuropathie nicht zugelassen ist, das wirksamste Medikament in dieser Indikation sein könnte. Eine Cochrane-Analyse konnte aufgrund derselben Datenbasis dagegen keine Evidenz für eine Wirksamkeit nachweisen (11).
Ausblick
Nachdem Ergebnisse von Studien vorliegen, die zuvor nicht verfügbar waren, erscheint eine Neubewertung der Studienlage und eine Revision der Leitlinien erforderlich. Bis dahin sollten vorzugsweise die zugelassenen Wirkstoffe aus den Gruppen der Antidepressiva und Antiepileptika eingesetzt werden. Die Auswahl des Wirkstoffs sollte sich an den Nebenwirkungen und Kontraindikationen orientieren.
Fazit für die Praxis
Die Therapie der schmerzhaften diabetischen Polyneuropathie ist häufig unbefriedigend, da die Wirksamkeit der zugelassenen Medikamente lediglich gering bis moderat ist und Nebenwirkungen nicht selten zum Abbruch der Behandlung führen. Die Bewertung einzelner Wirkstoffe erfolgt in unterschiedlichen Metaanalysen sehr different. Es ist Aufgabe der Fachgesellschaften, diese verwirrenden Widersprüche zu analysieren und dem Kliniker überarbeitete Leitlinien zur Verfügung zu stellen. Für Pregabalin liegen zahlreiche bisher nicht von Metaanalysen berücksichtige Daten vor, die zu einer Herabstufung der Effektstärke führen. Die Metaanalyse von Waldfogel und Mitarbeitern (1) macht wieder einmal deutlich, dass evidenzbasierte Medizin den Zugang zu den Ergebnissen aller, auch bisher nicht veröffentlichter Studien erfordert.
Interessenkonflikte
Ein Interessenkonflikt wird vom Autor verneint.
Literatur
- Waldfogel JM, Nesbit SA, Dy SM et al.: Pharmacotherapy for diabetic peripheral neuropathy pain and quality of life: A systematic review. Neurology 2017; 88: 1958-1967.
- Dyck PJ, Kratz KM, Karnes JL et al.: The prevalence by staged severity of various types of diabetic neuropathy, retinopathy, and nephropathy in a population-based cohort: the Rochester Diabetic Neuropathy Study. Neurology 1993; 43: 817-824.
- Edwards JL, Vincent AM, Cheng HT, Feldman EL: Diabetic neuropathy: mechanisms to management. Pharmacol Ther 2008; 120: 1-34.
- Diabetes C, Complications Trial Research G, Nathan DM et al.: The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med 1993; 329: 977-986.
- Finnerup NB, Sindrup SH, Jensen TS: The evidence for pharmacological treatment of neuropathic pain. Pain 2010; 150: 573-581.
- Nationale Versorgungsleitlinie: Neuropathie bei Diabetes im Erwachsenenalter. Langfassung:http://www.awmf.org/uploads/tx_szleitlinien/nvl-001e_l_S3_Diabetes_Neuropathie_2016-07.pdf
- Pop-Busui R, Boulton AJ, Feldman EL et al.: Diabetic Neuropathy: A Position Statement by the American Diabetes Association. Diabetes Care 2017; 40: 136-154.
- Bril V, England J, Franklin GM et al.: Evidence-based guideline: Treatment of painful diabetic neuropathy: report of the American Academy of Neurology, the American Association of Neuromuscular and Electrodiagnostic Medicine, and the American Academy of Physical Medicine and Rehabilitation. PM R 2011; 3: 345-352, 352 e341-321.
- Griebeler ML, Morey-Vargas OL, Brito JP et al.: Pharmacologic interventions for painful diabetic neuropathy: An umbrella systematic review and comparative effectiveness network meta-analysis. Ann Intern Med 2014; 161: 639-649.
- Wiffen PJ, Derry S, Bell RF et al.: Gabapentin for chronic neuropathic pain in adults. Cochrane Database Syst Rev 2017; Issue 6: CD007938.
- Gallagher HC, Gallagher RM, Butler M et al.: Venlafaxine for neuropathic pain in adults. Cochrane Database Syst Rev 2015; Issue 8: CD011091.
