Nicht lieferbar: Paracetamol- und Ibuprofen-haltige Fiebersäfte für Kinder
Das aktuelle Thema
(Dieser Artikel wurde am 18. August 2022 vorab online veröffentlicht.)
Paracetamol-Säfte als pädiatrische Darreichungsform sind seit Wochen in Deutschland nicht verfügbar und weder in den Vor-Ort-Apotheken noch im Versandhandel erhältlich. Theoretisch stünde Ibuprofen als Saft und Zäpfchen (z. B. Nurofen® und Generika) als eine mögliche Alternative zur Verfügung, allerdings sind diese mittlerweile, mutmaßlich infolge der Nichtverfügbarkeit von Paracetamol-Säften, auch nicht mehr erhältlich (1).
Information des BfArM
Im Zusammenhang mit der derzeitig eingeschränkten Verfügbarkeit von Fiebersäften hat das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) nach eigener Information umfangreiche Recherchen und Prüfungen durchgeführt. Als Gründe wurden dabei der Rückzug eines Marktteilnehmers und auch eine Verteilproblematik identifiziert (2). Ein Lieferabriss soll nach Kenntnis des BfArM zu keinem Zeitpunkt eingetreten sein und die in den Markt im Direktvertreib oder über den vollversorgenden Großhandel abgegebenen Warenmengen sollen in Summe den bisherigen durchschnittlichen Bedarf repräsentieren. Im Jahr 2022 sei der Bedarf an den betroffenen Arzneimitteln überproportional über den bisherigen durchschnittlichen Bedarf angestiegen, die Ursachen hierfür konnten aber bislang nicht befriedigend ermittelt werden.
In Abstimmung zwischen BfArM, dem GKV-Spitzenverband, der Kassenärztlichen Bundesvereinigung (KBV) und der ABDA – Bundesvereinigung Deutscher Apothekerverbände wurde daher als Kompensationsmaßnahme die Fertigung von individuellen Rezepturarzneimitteln auf ärztliche Verschreibung in Apotheken vorgeschlagen (2). Diese Maßnahme soll allerdings ausschließlich im Einzelfall zur Anwendung kommen, wenn der Krankheitszustand des Kindes eine Behandlung mit den in Rede stehenden Wirkstoffen erfordert.
Folgende Voraussetzungen wurden vereinbart:
- Der Fiebersaft wurde vom behandelnden Arzt / von der behandelnden Ärztin verschrieben.
- Die Nichtbeschaffbarkeit des verordneten Fertigarzneimittels ist in der Apotheke zu dokumentieren. Hierfür wird die Dokumentation in den Warenwirtschaftssystemen als ausreichend erachtet.
- Bei Nichtverfügbarkeit des verordneten Arzneimittels soll die Rücksprache zu medikamentösen Alternativen mit dem behandelnden Arzt / der behandelnden Ärztin erfolgen.
- Im Fall, dass die Gabe von Paracetamol- oder Ibuprofen-haltigen Fiebersäften medizinisch erforderlich ist, und mehrere Arzneimittel auf einem Rezept verordnet sind, ist ein neues Rezept über eine Rezeptur auszustellen.
Es wird Ärztinnen und Ärzten daher empfohlen, im Zeitraum der eingeschränkten Verfügbarkeit bei der Verordnung eines Paracetamol- oder Ibuprofen-haltigen Fiebersaftes jeweils ein separates Rezept auszustellen, das bei nicht Verfügbarkeit von der Apotheke mit einem Vermerk zur ersatzweisen Herstellung einer Rezeptur nach Rücksprache mit dem behandelnden Arzt/ der behandelnden Ärztin versehen wird.
- Die Taxierung der Rezeptur erfolgt nach Arzneimittelpreisverordnung. Dabei gelten die Regelungen der Hilfstaxe (Vertrag über die Preisbildung für Stoffe und Zubereitungen aus Stoffen (§§ 4 und 5 der AMPreisV).
- Das BfArM wird regelmäßig die Lieferfähigkeit der Unternehmen ermitteln und die Informationen zur Verfügung stellen.
- Der Nachweis einer längeren Nichtverfügbarkeit durch das BfArM kann einer regelmäßigen ärztlichen Verschreibung bei der Herstellung von Defekturen in der Apotheke gleichgesetzt werden.
- Der GKV-Spitzenverband wird die Krankenkassen informieren und dringend empfehlen, dass in dem Zeitraum der eingeschränkten Verfügbarkeit den Apotheken die Rezepturen von den gesetzlichen Krankenkassen erstattet werden.
- Die ärztlichen Verschreibungen sollen im Rahmen der Wirtschaftlichkeitsprüfung gesondert berücksichtigt werden.
Ein Defekturarzneimittel ist nach § 1a Absatz 9 ApBetrO ein Arzneimittel, das im Rahmen des üblichen Apothekenbetriebs im Voraus an einem Tag in bis zu 100 abgabefertigen Packungen oder in einer diesen entsprechenden Menge hergestellt wird. Die Herstellung in der Apotheke im Defekturmaßstab ist allerdings nach § 21 Abs. 2 Arzneimittelgesetz nur dann zulässig, wenn sie auf Grund nachweislich häufiger ärztlicher oder zahnärztlicher Verschreibung erfolgt.
Fertigarzneimittel auf dem Markt
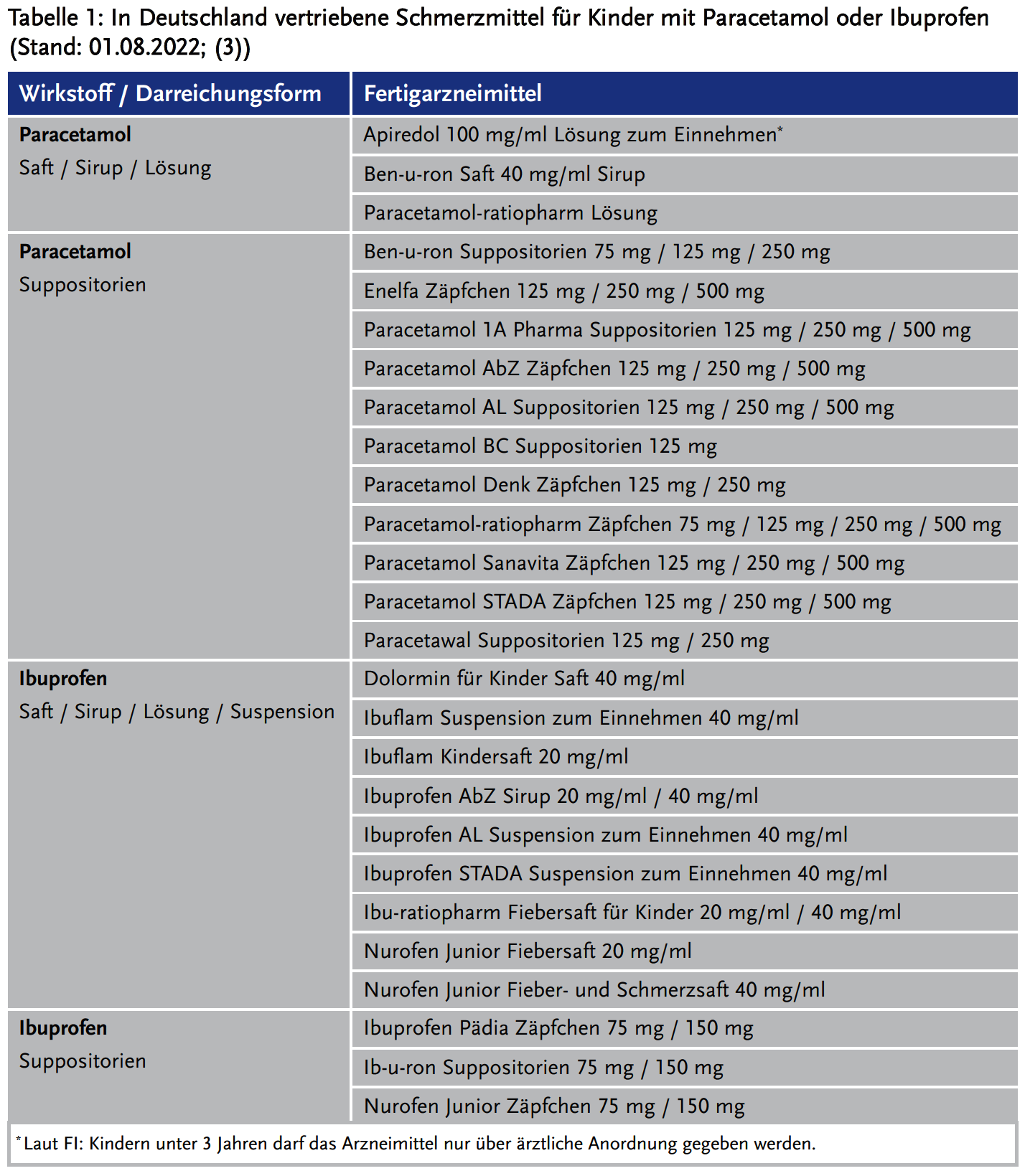
Paracetamol-Säfte werden derzeit nur noch von drei pharmazeutischen Unternehmern angeboten (siehe Tabelle 1); alle anderen Marktteilnehmer wie Paracetamol Saft Hexal® oder Paracetamol STADA Saft® sind seit längerer Zeit außer Vertrieb. Im Gegensatz dazu wird Ibuprofen-Saft zumindest von noch sieben pharmazeutischen Unternehmern vertrieben z. B. Nurofen Junior Fieber- und Schmerzsaft®, Dolormin für Kinder®, Ibuprofen AbZ Sirup®. Nicht viel besser ist die Marktlage bei den Zäpfchen: Paracetamol-Suppositorien für Kinder werden zwar von acht pharmazeutischen Unternehmern in unterschiedlichen Stärken (75–250 mg pro Zäpfchen) angeboten, Ibuprofen-Suppositorien aber nur von drei (75 bzw. 125 mg pro Zäpfchen) (siehe Tabelle 1) (3).
Weiterhin ist ein Pulver zum Einnehmen mit dem Wirkstoff Ibuprofen als Fertigarzneimittel in der Dosierung 200 oder 400 mg verfügbar, das wie Brausepulver direkt auf die Zunge gegeben wird. Das Pulver ist bei Kindern ab 20 kg Körpergewicht und sechs Jahren zugelassen (Ibu-Ratiopharm® direkt 200 mg Pulver zum Einnehmen). Dieses Arzneimittel lässt sich zudem nach Auskunft des Herstellers als Individualrezeptur zu Kapseln mit niedrigeren Dosierungen verarbeiten; die Kapseln können zur Verabreichung des Pulvers geöffnet werden (Quelle: persönliche Auskunft Ratiopharm).
Der pharmazeutische Unternehmer Ratiopharm, der Säfte und Zäpfchen mit Paracetamol und Ibuprofen vertreibt, kämpft derzeit wohl auch mit Lieferengpässen aufgrund von unerwartetem und stark erhöhtem Bedarf im Markt sowie Lieferverzögerungen seitens der Wirkstoffproduzenten. Laut eigener Auskunft stünden ihm derzeit keine Lagerbestände von Kinderschmerzmitteln zur Verfügung, die Produktion laufe aber auf Hochtouren (4).
Engpässe auch bei Elotrans® und Oralpädon®
Seit einigen Wochen sind zudem Fertigarzneimittel zur Rehydratation und Elektrolytsubstitution bei Durchfallerkrankungen nicht mehr erhältlich. Elotrans® und Oralpädon® beinhalten Glukose-Elektrolyt-Mischungen zur Herstellung einer Lösung zur Einnahme und werden bei Durchfallerkrankungen eingesetzt. Diese sind nach der Arzneimittel-Richtlinie (5) für Säuglinge, Kleinkinder und Kinder bis zum vollendeten 12. Lebensjahr zu Lasten der gesetzlichen Krankenversicherung verordnungsfähig. Als Grund für die Nichtverfügbarkeit wird eine stark erhöhte Nachfrage angenommen, da in den sozialen Medien Elotrans® als neues Wundermittel gegen Beschwerden nach exzessivem Alkoholkonsum angepriesen worden sei. Damit solle Elektrolytverlusten aufgrund der diuretischen Alkoholwirkung entgegengewirkt und einem „Kater“ vorgebeugt werden (6). Auch hier können Apotheken Abhilfe schaffen, indem sie entsprechende Glukose-Elektrolyt-Pulvermischungen als Rezeptur herstellen.
Produkte wie Humana Elektrolyt und HiPP PRS 200, die als orale Rehydrationslösungen bei Durchfällen von Kleinkindern und Kindern angeboten werden, sind Lebensmittel und nicht auf Kassenrezept verordnungsfähig. Infectodiarrstop LGG® enthält eine Wirkstoffkombination aus Laktobazillen (Lactobacillus rhamnosus GG) und einer oralen Rehydratationslösung und zählt damit zu den Antidiarrhoika, für die von den wenigen, explizit genannten Ausnahmen abgesehen, eine Verordnung auch für Kinder bis zum vollendeten 12. Lebensjahr und für Jugendliche mit Entwicklungsstörungen bis zum vollendeten 18. Lebensjahr unwirtschaftlich ist (5).
BfArM-Liste zu aktuellen Lieferengpässen
Das BfArM stellt seit einigen Jahren der Öffentlichkeit Informationen zu gemeldeten Lieferengpässen zur Verfügung. Die Informationen stammen vom pharmazeutischen Unternehmer und werden durch Daten aus der Arzneimittel- und Antragsdatenbank (AmAnDa) des Bundes ergänzt. Die Meldungen erfolgen durch die pharmazeutischen Unternehmer auf Basis einer Selbstverpflichtung (7). In dieser Liste findet sich derzeit nur eine Meldung zu Lieferengpässen für Paracetamol- oder Ibuprofen-haltigen Säften bzw. Suppositorien: Ibuflam® Kindersaft 20 mg/ml.
Das liegt daran, dass diese Selbstverpflichtung zur Meldung nach den derzeit vereinbarten Kriterien nur für Arzneimittel mit Wirkstoffen gilt, die als versorgungskritisch eingestuft wurden. Folgende Kriterien definieren versorgungskritische Wirkstoffe gemäß § 52b Absatz 3c AMG:
Die Wirkstoffe sind als versorgungsrelevant eingestuft und
- für sie sind im Arzneimittelinformationssystem des Bundes drei oder wenige
- Zulassungsinhaber oder
- endfreigebende Hersteller oder
- Wirkstoffhersteller für verkehrsfähige Arzneimittel hinterlegt oder
- für sie ist bereits in der Vergangenheit ein Versorgungsmangel eingetreten oder
- sie werden auf der Substitutionsausschlussliste geführt.
In einer Liste sind die versorgungskritischen Wirkstoffe aufgeführt, die den genannten Kriterien entsprechen.
Paracetamol und Ibuprofen gelten nicht als versorgungsrelevant oder versorgungskritisch, sodass derzeit bestehende Lieferengpässe für Paracetamol- und Ibuprofen-haltige Fiebersäfte für Kinder nicht im Sinne der Selbstverpflichtung gemeldet werden müssen. Ein Grund dafür ist, dass der Beirat zu Liefer- und Versorgungsengpässen zur Definition der versorgungsrelevanten Wirkstoffe unter anderem beschlossen hat, dass OTC-Arzneimittel grundsätzlich nicht als versorgungsrelevant gelten. Allerdings könne laut BfArM generell jeder Lieferengpass an das BfArM gemeldet werden wie im Beispiel Ibuflam® Kindersaft.
Definition versorgungsrelevante Wirkstoffe (8):
Die Liste der versorgungsrelevanten Wirkstoffe nach § 52b Abs. 3c AMG wurde auf der Basis der Vorschläge der medizinischen Fachgesellschaften und der WHO-Liste der essenziellen Arzneimittel zusammengeführt und wird regelmäßig auf Aktualität geprüft und sofern erforderlich angepasst. Grundsätzliche Voraussetzung für die Versorgungsrelevanz eines Wirkstoffes bzw. einer Wirkstoffkombination ist, dass die Arzneimittel verschreibungspflichtig sind und dass der Wirkstoff für die Gesamtbevölkerung relevant ist.
Weitere Kriterien zur Identifizierung von versorgungsrelevanten Arzneimitteln sind:
- Für das Arzneimittel gibt es aktuell keine gleichwertige Alternative.
- Bei Nichtverfügbarkeit verschlechtert sich die Prognose der betroffenen Patientinnen und Patienten.
- Das Arzneimittel wird in inhaltlich aktuellen Leitlinien der Fachgesellschaften empfohlen bzw. es entspricht dem aktuellen Therapiestandard.
- Die zu behandelnde Krankheit ist lebensbedrohlich oder irreversibel progredient oder bei fehlender Behandlung würden betroffene Patientinnen und Patienten schwer geschädigt. Dies gilt sowohl für Akutsituationen (Notfall), chronische Situationen oder Situationen mit einem möglichen tödlichen Verlauf, in denen das Arzneimittel den Verlauf positiv beeinflusst.
Fazit für die Praxis
- Fiebersäfte mit Ibuprofen oder Paracetamol sind derzeit in Deutschland weitestgehend nicht verfügbar.
- Die Fertigung von individuellen Rezepturarzneimitteln mit diesen Wirkstoffen auf ärztliche Verschreibung in Apotheken soll als Kompensationsmaßnahme den Versorgungsengpass überbrücken.
- Es wird Ärztinnen und Ärzten daher empfohlen, im Zeitraum der eingeschränkten Verfügbarkeit bei der Verordnung eines Paracetamol- oder Ibuprofen-haltigen Fiebersaftes jeweils ein separates Rezept auszustellen.
- Suppositorien mit Ibuprofen oder Paracetamol sollen derzeit noch verfügbar sein, wenn auch bereits regional eingeschränkt.
Literatur
- Nicht versorgungsrelevant?! Warum Paracetamol-Saft nicht auf der Engpassliste des BfArM auftaucht. DAZ 2022; 162 (Heft 30): 10.
- Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM): Aktuelle Informationen des BfArM zur eingeschränkten Verfügbarkeit von Paracetamol- und Ibuprofen-haltigen Fiebersäften für Kinder: https://www.bfarm.de/DE/Arzneimittel/Arzneimittelinformationen/Lieferengpaesse/mitteilung_fiebersaefte_kinder.html;jsessionid=C5EB05AD6B6A07F673AAB77F9717E98C.intranet251 (letzter Zugriff: 5. August 2022). Bonn, 2. August 2022.
- Lauer-Taxe, Stand: 1. August 2022.
- Keine Winterbevorratung mit Ratiopharm. Folge des Engpasses bei Kinder-Schmerzmitteln. DAZ 2022; 162 (Heft 29): 14.
- Arzneimittel-Richtlinie, Anlage III: Übersicht über Verordnungseinschränkungen und -ausschlüsse in der Arzneimittelversorgung durch die Arzneimittel-Richtlinie und aufgrund anderer Vorschriften (§ 34 Absatz 1 Satz 6 und Absatz 3 SGB V), Hinweise zur wirtschaftlichen Verordnungsweise von nicht verschreibungspflichtigen Arzneimitteln für Kinder bis zum vollendeten 12. Lebensjahr und für Jugendliche mit Entwicklungsstörungen bis zum vollendeten 18. Lebensjahr sowie Verordnungseinschränkungen und -ausschlüsse von sonstigen Produkten: https://www.g-ba.de/downloads/83-691-714/AM-RL-III-Verordnungseinschraenkung_2022-01-18.pdf (letzter Zugriff: 5. August 2022. Stand: 18. Januar 2022.
- Bergner A. Engpässe bei Elotrans und Oralpädon. Welche Rezepturen als Alternative dienen können. DAZ 2022; 162 (Heft 30): 18-21.
- PharmNet.Bund: Veröffentlichte Lieferengpassmeldungen: https://anwendungen.pharmnet-bund.de/lieferengpassmeldungen/faces/public/meldungen.xhtml. Letzter Zugriff: 5. August 2022.
- Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM): Liste der versorgungsrelevanten Wirkstoffe: https://www.bfarm.de/DE/Arzneimittel/Arzneimittelinformationen/Lieferengpaesse/Liste-Wirkstoffe-versorgungsrelevant/_node.html (letzter Zugriff: 5. August 2022). Stand: 6. April 2022.
Interessenkonflikte
Die Autoren erklären, keine Interessenkonflikte zu haben.
