Therapie mit peroralen Antibiotika bei Störungen der Nierenfunktion
Oral antibiotic therapy in renal failure
Zusammenfassung
Eine antiinfektive Therapie bei chronischer Niereninsuffizienz stellt Ärzte in der Praxis oft vor eine Herausforderung. Dieser Artikel soll daher eine Übersicht über gängige Prinzipien zur Risikoeinschätzung und Dosisanpassung von peroralen Antibiotika bei gestörter Nierenfunktion geben. Direkt nephrotoxische Medikamente sind von denen mit anderen unerwünschten Arzneimittelwirkungen in Bezug auf die Nieren zu unterscheiden.
Abstract
Dose adjustment of anti-infective medication to renal function is a common problem in clinical practice. This review is supposed to give a short overview about risks and dose adjustment of oral antibiotics for patients with impaired kidney function. Direct nephrotoxic effects should be distinguished from other adverse events affecting the kidneys.
Eine Verordnung von Antibiotika bei Patienten mit Nierenfunktionsstörung stellt den niedergelassenen Arzt immer wieder vor eine Herausforderung. Auf Grund der hohen Prävalenz von klinisch relevanten Funktionseinschränkungen (1) ist es für jeden praktizierenden Arzt von Vorteil, die Dosierung von gängigen Antiinfektiva bei Niereninsuffizienz zu kennen. In diesem Artikel soll eine Zusammenfassung über die Dosierung der wichtigsten peroralen Antibiotikaklassen bei den verschiedenen Stadien der chronischen Niereninsuffizienz gegeben werden.
Die meisten Dosierungsempfehlungen für Niereninsuffizienz gelten für die Kreatinin-Clearance (CrCl) berechnet mit der Cockcroft-Gault-Formel (2). Diese Formel hat den Vorteil, dass das Körpergewicht des Patienten in die Berechnung miteinbezogen wird und damit eine Schätzung in ml/min erfolgt. Von KDIGO (Kidney Disease: Improving Global Outcomes) wird seit 2011 die Nutzung der weit verbreiteten MDRD- oder CKD-EPI-Formeln zur Schätzung der glomerulären Filtrationsrate (GFR) empfohlen, da die Ergebnisse meist besser mit der tatsächlichen GFR übereinstimmen (3); allerdings sind diese Werte auf eine durchschnittliche Körperoberfläche von 1,73m2 normalisiert (Einheit ml/min/1,73m2). Dies ist zur Diagnose einer chronischen Nierenerkrankung sinnvoll („kleine Menschen haben kleine Nieren“), theoretische Argumente sprechen aber dafür, einen absoluten Wert in ml/min für die Arzneimitteldosierung zu verwenden. Die Überlegenheit einer dieser Berechnungsmethoden in Bezug auf Medikamentendosierung konnte jedoch bisher nicht nachgewiesen werden (3). Die Ergebnisse der eGFR nach MDRD- oder CKD-EPI-Formel stehen jedoch meistens automatisch durch das Labor bereit und müssen nicht noch selbst berechnet werden. Im Grenzfall sollte eine Recherche bezüglich der Formel für die Zulassung des Medikaments (siehe Fachinformation) sowie eine klinische Abwägung erfolgen. Im akuten Nierenversagen gilt größere Vorsicht, da es zu starken Schwankungen der glomerulären Filtrationsrate kommen kann und eine Berechnung mit den genannten Formeln nicht zuverlässig ist (da sich das Serum-Kreatinin nicht im „Steady-State“ befindet). Des Weiteren ist zu beachten, dass das Serum-Kreatinin nicht immer die reale Nierenfunktion widerspiegelt. So liegt eine leichte Nierenfunktionseinschränkung oft noch im „kreatininblinden“ Bereich (4). Anurische Patienten haben natürlich (trotz rechnerisch meist höher geschätzter GFR) effektiv eine GFR von 0 ml/min.
Generell sollten bei Nierenfunktionseinschränkung Substanzen ohne Nephrotoxizität sowie mit großer therapeutischer Breite gewählt werden. Natürlich ist dies, nicht zuletzt wegen steigender Resistenzentwicklungen, nicht immer möglich (5). Liegt ein Antibiogramm vor, ist selbstverständlich die Therapie mit dem stärksten Nutzen in Abwägung mit dem nierenschädigenden Potenzial sowie der geeigneten Dosis auszuwählen. Es sollte auch bedacht werden, dass mögliche Nebenwirkungen durch Überdosierung sowie Nephrotoxizität der Gefahr der Unterdosierung bei zu ausgeprägter Dosisanpassung gegenüberstehen. Im ambulanten Bereich hat dies zwar meist nicht die gleichen Konsequenzen wie zum Beispiel bei Patienten im septischen Schock, sollte jedoch trotzdem nicht außer Acht gelassen werden. Bei schwer kranken Patienten sollte man die antiinfektive Therapie eher im oberen Bereich der möglichen Dosierung verabreichen. Ist der Patient dialysepflichtig, sollten Antibiotika gewählt werden, für die es Daten bezüglich der Elimination an Hämo- bzw. Peritonealdialyse gibt.
Besondere Vorsicht ist bei potenziell nephrotoxischen Medikamenten geboten, wie zum Beispiel Aminoglykosiden, um eine bestehende Nierenfunktionseinschränkung nicht noch weiter zu verschlechtern. Außerhalb der direkten Nephrotoxizität gibt es auch Medikamente, die eine Nierenschädigung über andere Mechanismen hervorrufen können (6). Die interstitielle Nephritis, nicht selten unter ß-Lactamen beobachtet, kann eine Nierenfunktionsverschlechterung hervorrufen, die nicht durch direkt toxische, sondern allergisch bedingte Mechanismen hervorgerufen wird (7). Klassischerweise macht sich diese durch einen Anstieg der Retentionsparameter bemerkbar. Im Urin findet sich oft eine sterile Leukozyturie. Eosinophilie im Serum oder Urin sowie ein erhöhtes IgE können Hinweise auf eine interstitielle Nephritis sein. Beweisend ist letztendlich jedoch nur eine Nierenbiopsie. Gelegentlich wird diese unerwünschte Arzneimittelwirkung (UAW) auch mit „Hautausschlag der Niere“ betitelt. Bei der Auswahl eines Antibiotikums wird jedoch nur die direkte Nephrotoxizität berücksichtigt.
Unabhängig von den nötigen Dosisanpassungen auf Grund der Pharmakokinetik sind auch andere UAW zu beachten, die bei Niereninsuffizienz besonders relevant sind. Patienten mit einer vorbekannten Nierenschädigung sind oft vulnerabler für solche Effekte. So ist zum Beispiel Vorsicht geboten bei Cotrimoxazol oder Trimethoprim, da diese Hyperkaliämien verursachen können. Die Wahrscheinlichkeit hierfür ist bei chronischer Niereninsuffizienz deutlich erhöht und ein entsprechendes Monitoring der Elektrolyte sollte durchgeführt werden.
Wird ein überwiegend renal eliminiertes Medikament bei Niereninsuffizienz gegeben, so verlängert sich die Halbwertszeit und bei regelmäßiger Anwendung erhöhen sich die Plasmaspiegel. Trotzdem sind Antibiotika, die überwiegend renal eliminiert werden, nicht automatisch kontraindiziert. Bei Vancomycin, aber auch bei Aminoglykosiden, sollten Talspiegelbestimmungen die Dosierung begleiten. Die „Loading dose“ sollte unabhängig von der Nierenfunktion immer gleich gewählt werden (Ausnahme: Aminoglykoside bei hochgradiger Niereninsuffizienz). Die Erhaltungsdosis wird dann je nach Nierenfunktion auf Grund der verzögerten renalen Elimination oder auf Grund der gemessenen Konzentrationen angepasst. Wirken Antibiotika eher über einen konstanten Spiegel (relevanter Wirkparameter: Zeit in der die Konzentration oberhalb der minimalen Hemmkonzentration liegt), wie zum Beispiel ß-Lactame, sollten die Dosierungsintervalle eher beibehalten und die Einzeldosis reduziert werden, um einen gleichbleibenden Plasmaspiegel zu gewährleisten. Wird die Wirkung eher durch Spitzenspiegel (zum Beispiel bei Gyrasehemmern oder Aminoglykosiden) bestimmt, empfiehlt sich eher eine Verlängerung des Intervalls zur nächsten Gabe bei normaler Einzeldosis (8).
Andere Antibiotika, wie zum Beispiel Ciprofloxacin oder Ceftriaxon, werden teils renal (ca. 50 %), teils hepatisch ausgeschieden bzw. metabolisiert (8). Hier wird eine Dosisanpassung erst bei weit fortgeschrittener Niereninsuffizienz empfohlen.
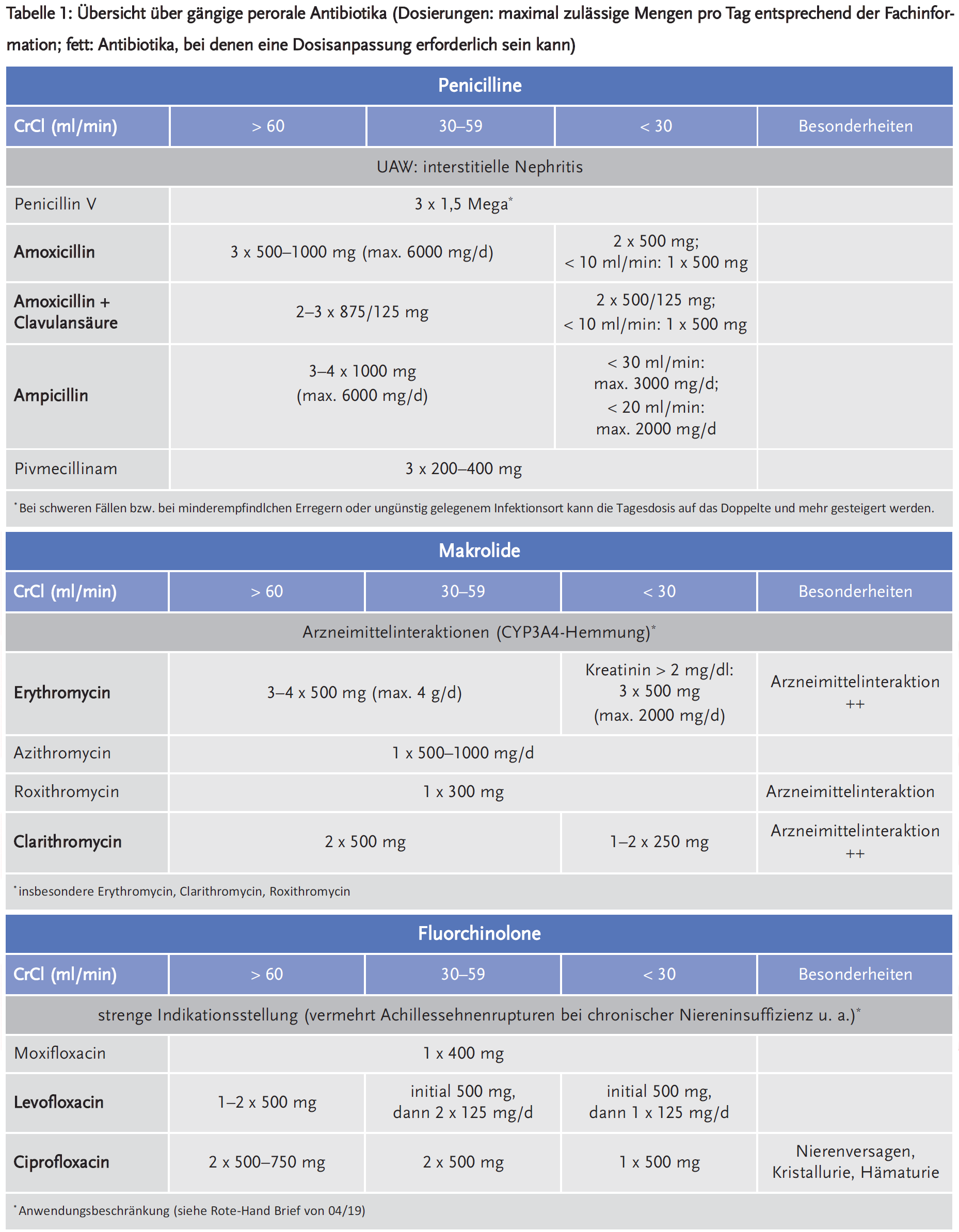
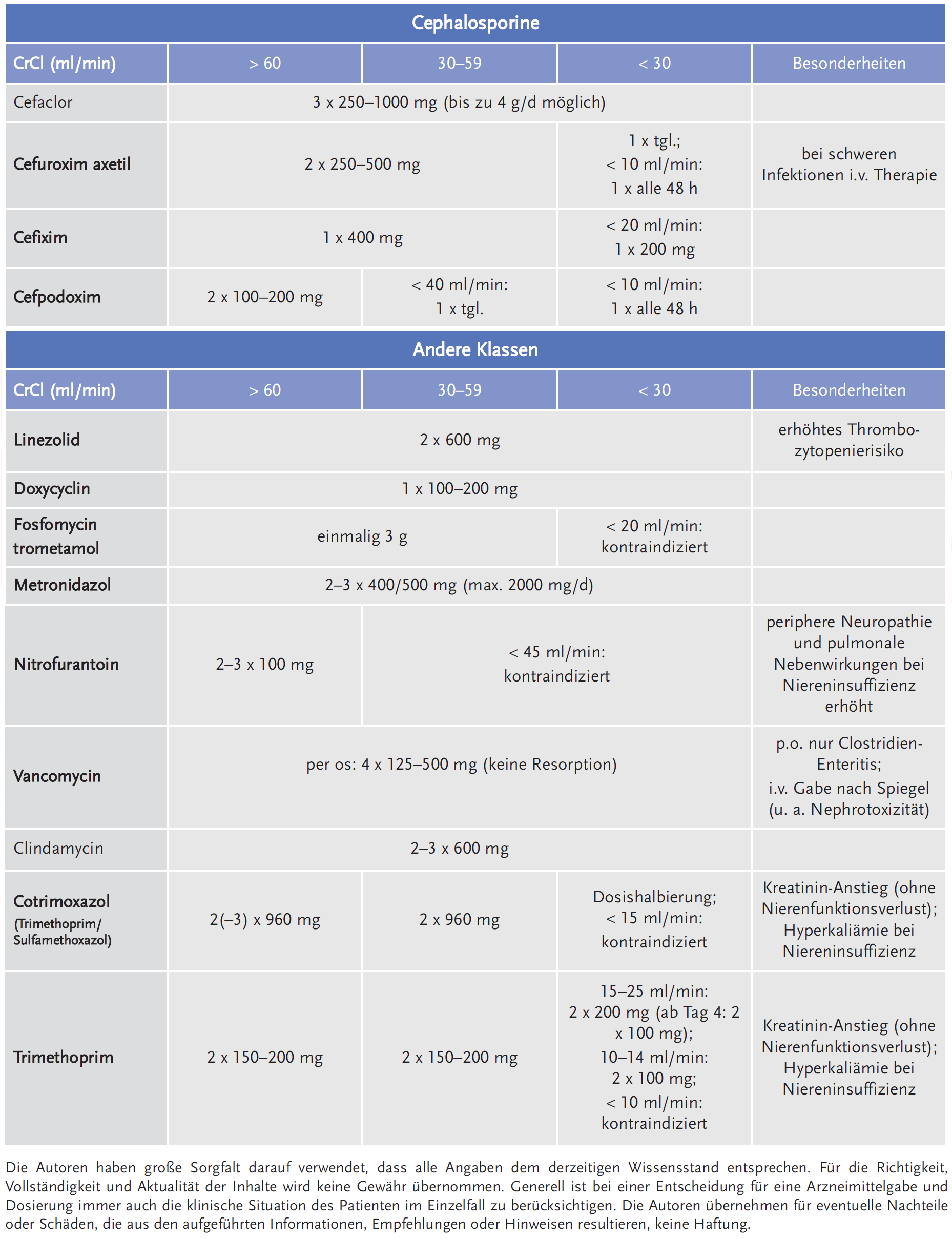
Im Folgenden wird eine Übersicht zu gängigen peroralen Antibiotika gegeben (Tabelle 1). Die Dosierungen beziehen sich auf maximal zulässige Mengen pro Tag (entsprechend der Fachinformation). Fett gedruckt sind Antibiotika, bei denen eine Dosisanpassung erforderlich sein kann. Die letztendliche Dosiswahl sollte auch immer unter Anbetracht der klinischen Schwere des Infektes erfolgen und kann deshalb im Einzelfall (bei sehr schweren Infekten) manchmal auch höher gewählt werden.
Generell sind bei allen unten genannten Antibiotika Arzneimittelinteraktionen möglich. Ebenfalls können fast alle dieser Medikamente interstitielle Nephritiden hervorrufen. Antibiotika, die dies besonders häufig tun, sind im Folgenden gekennzeichnet. Die absolute Häufigkeit ist jedoch gering.
Bei Unsicherheiten über die Dosierung von Medikamenten bei Niereninsuffizienz ist eine geeignete Seite zur Recherche https://www.dosing.de. Hier kann die geschätzte Nierenfunktion anhand von Alter, Gewicht, Geschlecht und Serum-Kreatinin berechnet werden. Anhand dessen werden Empfehlungen zur Dosisanpassung des gewählten Medikaments gegeben. Des Weiteren finden sich dort Hinweise zum Vorgehen bei Patienten mit Nierenersatztherapie und zu möglichen UAW an den Nieren.
Fazit für die Praxis
Bei niereninsuffizienten Patienten sollten wenn möglich Antibiotika verwendet werden, die eine große therapeutische Breite haben und für die es Empfehlungen zum Einsatz bei Niereninsuffizienz gibt. Bei dringlicher Indikation und Fehlen von gleichwertigen Alternativen kann aber so gut wie jedes Antibiotikum auch bei Niereninsuffizienz angewendet werden. Ist man sich darüber unsicher, hilft ein Blick auf https://www.dosing.de oder eine Anfrage in einer benachbarten nephrologischen Praxis oder Klinik.
Interessenkonflikte
Ein Interessenkonflikt wird von den Autoren verneint.
Literatur
- Girndt M, Trocchi P, Scheidt-Nave C et al.: The prevalence of renal failure. Results from the German Health Interview and Examination Survey for Adults, 2008–2011 (DEGS1). Dtsch Arztebl Int 2016; 113: 85-91.
- Cockcroft DW, Gault MH: Prediction of creatinine clearance from serum creatinine. Nephron 1976; 16: 31-41.
- Matzke GR, Aronoff GR, Atkinson AJ, Jr. et al.: Drug dosing consideration in patients with acute and chronic kidney disease-a clinical update from Kidney Disease: Improving Global Outcomes (KDIGO). Kidney Int 2011; 80: 1122-1137.
- Meeusen JW, Lieske JC: Looking for a better creatinine. Clin Chem 2014; 60: 1036-1039.
- Cassini A, Hogberg LD, Plachouras D et al.: Attributable deaths and disability-adjusted life-years caused by infections with antibiotic-resistant bacteria in the EU and the European Economic Area in 2015: a population-level modelling analysis. Lancet Infect Dis 2019; 19: 56-66.
- Czock D, Keller F: Arzneimittelinduzierte Nephrotoxizität. In: Haase M, Haase-Fielitz A (Hrsg.). Akute Nierenschädigung. 1. Aufl.; Heidelberg: Springer-Verlag, 2015; 117-131.
- Raghavan R, Shawar S: Mechanisms of drug-induced interstitial nephritis. Adv Chronic Kidney Dis 2017; 24(2): 64-71.
- Hartmann B, Czock D, Keller F: Drug therapy in patients with chronic renal failure. Dtsch Arztebl Int 2010; 107: 647-655; quiz 655-646.
