Schluckstörungen im Alter – Presby(dys)phagie
Dysphagia in the elderly
Zusammenfassung
Können altersphysiologische Veränderungen des Schluckaktes (Presbyphagie) nicht mehr kompensiert werden, spricht man von Presbydysphagie. Ursachen sind verminderte Geruchs- und Geschmackswahrnehmungen, Mundtrockenheit, Sarkopenie, verminderte Sensibilität im Mund-Rachen-Raum mit verzögerter Triggerung des Schluckreflexes und Veränderungen des Achsenskelett sowie des Bindegewebes. Konsekutiv kann es zu Malnutrition, ungewolltem Gewichtsverlust, bronchopulmonale Infekten und Aspirationspneumonien, Wirkverlust oraler Medikation, aber auch zu einem sozialen Rückzug kommen. Anamnese und klinische Untersuchung sind Basis einer durch Spezialverfahren ergänzten Diagnostik. Eine individualisierte Schlucktherapie sollte logopädische Übungstherapien, posturale Manöver und die Bolusmodifikation inkludieren.
Abstract
Presbydysphagia means decompensation of age-related changes of swallowing (presbyphagia). Causes are a decreased smell and taste perception, oral dryness, sarkopenia, decreased sensitivity in the oral revenge space with delayed triggering of the swallow reflex and changes of the axis skeleton as well as the bandage fabric. Consequences may be malnutrition, unintentional weight loss, bronchopulmonal infections and pneumonia, insufficient uptake of oral medication, but also social retreat. Anamnesis and clinical investigation are a basic for a differentiated diagnostics approach. An individualized therapy consists of logopaedics, posturale manoeuvres and the bolus modification.
Hintergrund
Das Risiko unter einer Schluckstörung zu leiden steigt mit zunehmendem Lebensalter deutlich an. Etwa 14 % aller älteren Menschen, die ein unabhängiges Leben führen (1), und über die Hälfte aller Pflegeheimbewohner sind von einer Dysphagie betroffen (2). Im Hinblick auf den demographischen Wandel kommt der Schluckstörung im Alter im klinischen Alltag eine wachsende Bedeutung zu.
Trotz einer hohen Prävalenz berichten nur wenige Patienten aktiv über dysphagische Beschwerden, da diese von den Betroffenen selbst nicht oder meist erst sehr spät bemerkt werden (3). Außerdem wird eine Schluckstörung, die sich im höheren Lebensalter manifestiert, häufig von den Betroffenen nicht als Erkrankung wahrgenommen, sondern als normale und unvermeidliche Begleiterscheinung des Alterns verstanden.
Die Dysphagie im höheren Lebensalter stellt einen unabhängigen Prädiktor für schwerwiegende Komplikationen dar und geht mit einem erhöhten Mortalitätsrisiko einher (4). Betroffene Patienten haben u. a. ein höheres Risiko unter Aspirationspneumonien, Malnutrition und Einbußen in der Lebensqualität zu leiden (5).
Begriffserläuterungen
Vielfältige altersbedingte anatomische und neurophysiologische Veränderungsprozesse wie Muskelabbau (Sarkopenie), Skelettveränderungen, Elastizitätsverlust des Bindegewebes und neuronale Funktionsverluste in Sensibilität, Sensorik und zentraler Regulation verursachen eine Modifikation des Schluckens, bei der alle Phasen des Schluckaktes betroffen sind. Diese altersphysiologischen Veränderungen entstehen in der Regel langsam, können zunächst noch kompensiert werden und können als primäre Presbyphagie bezeichnet werden (6-9). Während der primären Presbyphagie selbst kein Krankheitswert zukommt, kann bei Erschöpfung der Kompensationsreserven und damit einhergehender Dysphagie von einer sogenannten Presbydysphagie gesprochen werden.
Treten zusätzlich zu einer primären Presbyphagie mit verminderter Kompensationsreserve des Schluckaktes mit Dysphagien assoziierte Erkrankungen wie z. B. Morbus Parkinson, Hirninfarkte oder Demenz auf, kann dies als sekundäre Presbyphagie bezeichnet werden. Diese krankheitsbedingten Störungen können dann sehr viel rascher zu einer schweren Dysphagie führen als bei vergleichsweise jüngeren Menschen (4).
Der Schluckakt
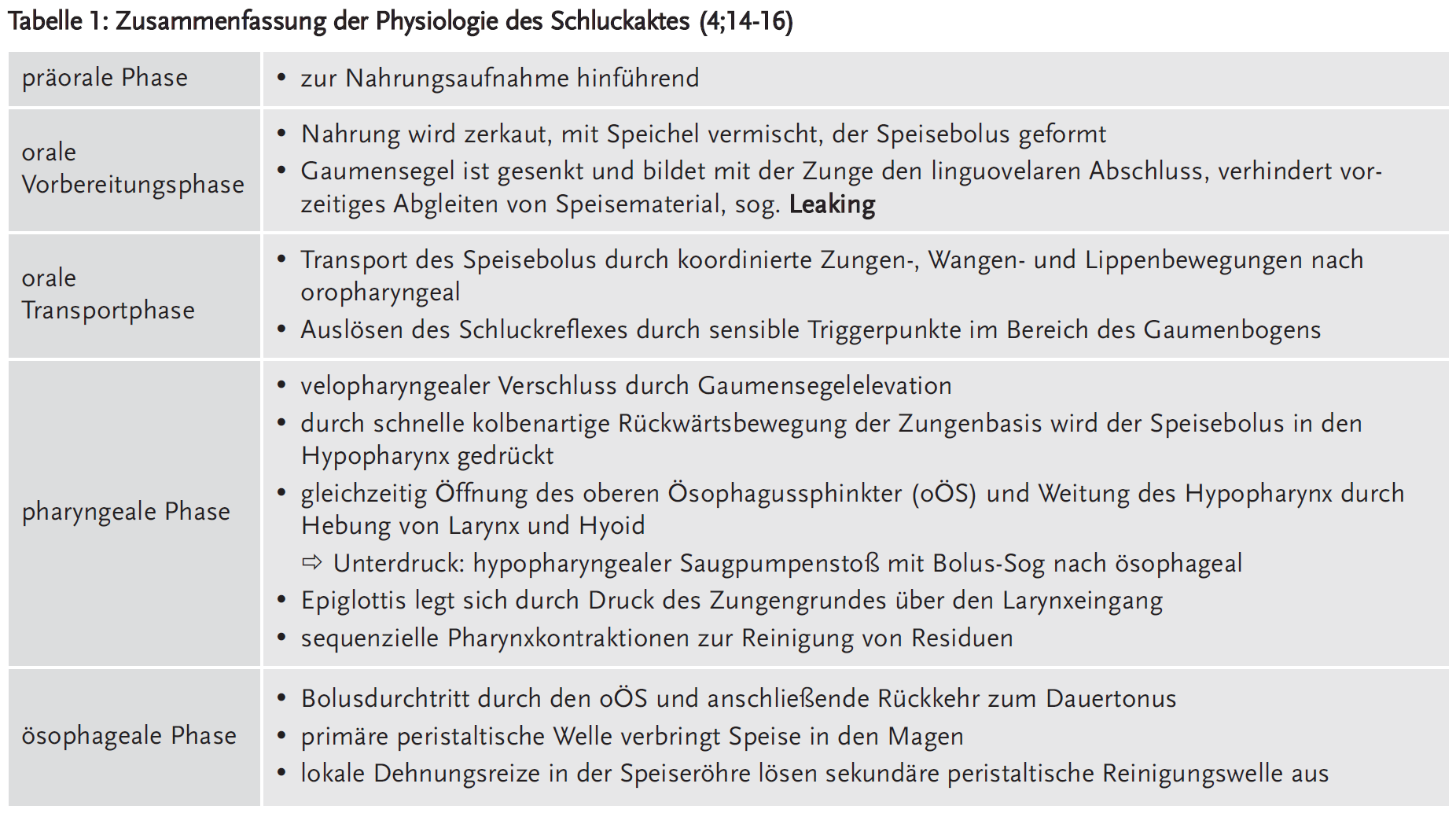
Der Schluckakt dient dem Transport von Nahrung und Speichel von der Mundhöhle in den Magen unter gleichzeitigem Schutz der Atemwege. Er kann in vier, wenn man die präorale Phase hinzuzählt, in fünf Phasen eingeteilt werden. Der Ablauf erfordert die bilaterale, koordinierte Aktivierung und Inhibition von mehr als 25 Muskelpaaren in der Mundhöhle, Rachen, Kehlkopf und Speiseröhre. Hierbei sind fünf Hirnnerven sowie die Ansa cervicalis (C1-C3) beteiligt (4;11;16).
Die überwiegend willkürliche orale Vorbereitungsphase, die orale Phase sowie die reflektorische pharyngeale Phase unterliegen einer somatischen Innervation (quergestreifte Muskulatur). Die Ösophagusperistaltik wird neben intrinsischen Vorgängen durch den „dorsalen Vaguskomplex“ der Medulla oblongata gesteuert, die Innervation der glatten Ösophagusmuskulatur erfolgt durch das autonome Nervensystem (12). Die zentralnervöse Steuerung des Schluckaktes ist ebenfalls komplex und umfasst neben den Schluckzentren des Hirnstamms ein ausgedehntes supramedulläres Schlucknetzwerk (einbezogen sind u. a. Insel, Gyrus cinguli, Stammganglien, prämotorische Areale und der primäre sensomotorische Kortex) (13;14).
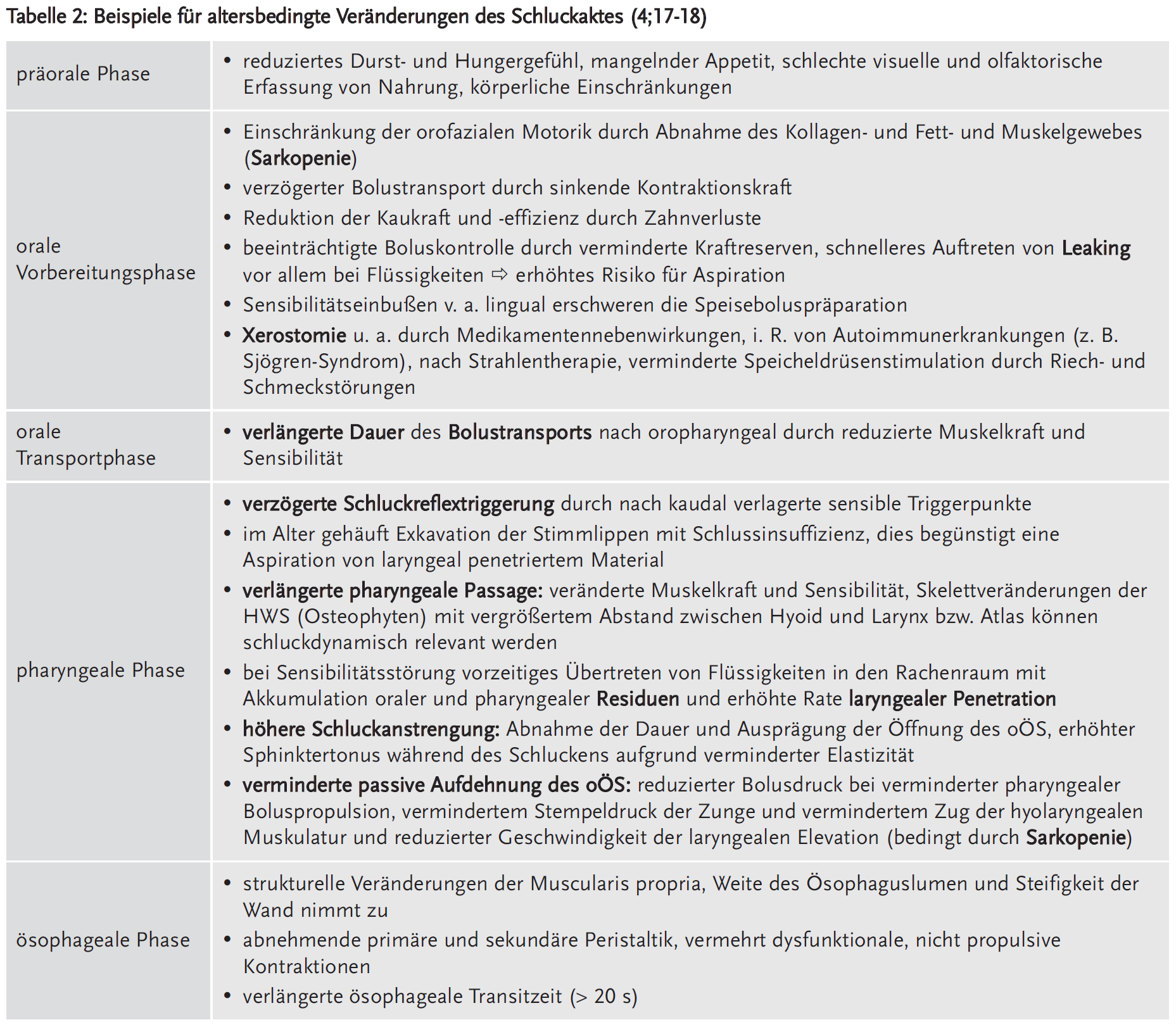
Altersbedingte Veränderungen betreffen alle Phasen des Schluckaktes. Dabei beeinträchtigen z. B. verminderte Geruchs- und Geschmackswahrnehmung sowie Mundtrockenheit die orale Vorbereitungsphase. Eine Sarkopenie alteriert alle motorischen Komponenten des Schluckaktes. Verminderte Sensibilität im Mund-Rachen-Raum kann zu einer verzögerten Schluckreflextriggerung führen. Zudem wird der gesamte Schluckbewegungsablauf durch Veränderungen des Achsenskelettes und des Bindegewebes beeinflusst (4;14-18) (Details siehe Tabellen 1 und 2).
Anamnese
Schluckprobleme werden selten spontan von Patienten angegeben. So sollte vor allem bei gehäuft auftretenden bronchopulmonalen Infekten, ungewolltem Gewichtsverlust, Malnutrition oder einem Wirkverlust oral einzunehmender Medikamente eine dysphagische Problematik in Betracht gezogen werden (11). Gezielt sollte nach Symptomen und ggf. veränderten Verhaltensweisen gefragt werden (Tabelle 3).

Der Zeitpunkt des Auftretens der Symptome vor, während oder nach dem Schlucken, kann Hinweise auf die betroffene Schluckphase geben. Beobachtungen von Angehörigen können ebenfalls Hinweise liefern (20).
Diagnostik
Differenzialdiagnostisch sollten von einer Presbydysphagie Erkrankungen mit dysphagischen Symptomen und ggf. spezifischen Therapieoptionen abgegrenzt werden. Patienten mit HNO-Erkrankungen und Tumoren weisen gehäuft eine Dysphagie auf. Im Rahmen vieler neurologischer Erkrankungen wie z. B. Morbus Parkinson und Schlaganfällen kann es zu einer neurogenen Dysphagie kommen. Auch internistische Erkrankungen (z. B. Motilitätstörungen des Ösophagus, Neoplasien des Ösophagus/Mediastinums/zentralen Bronchialsystems, entzündliche Speiseröhrenerkrankungen und Stenosen, Divertikel, postoperative Zustände, Autoimmunerkrankungen mit Xerostomie etc.) (21), dentale, psychiatrische oder orthopädische Erkrankungen können Auslöser einer Dysphagie sein (11).
Zunächst kann eine klinische Untersuchung von Mundhöhle, Gaumensegel und Rachenhinterwand Hinweise auf strukturelle und muskuläre Veränderungen in Mundhöhle und Pharynx, Sensibilitätsstörungen der Gaumenbögen, Schleimhautbeschaffenheit und -befeuchtung und Zahnstatus liefern (20).
Mittels klassischer transoraler Laryngoskopie lassen sich bereits auffällige Speichelansammlungen in Kehlkopf und Pharynx und postdeglutitive Speisereste erkennen (20). Die transnasale flexible endoskopische Evaluation des Schluckaktes (FEES) stellt die gängigste Methode zur objektiven Beurteilung des Schluckaktes dar (19). Vorteilhaft ist, dass die FEES auch ambulant und ggf. mobil (bettlägerige Patienten) durchführbar ist. Bestandteil einer FEES sind die Beurteilung der Strukturen in Ruhe, die Funktionsprüfung ohne und mit Nahrungsaufnahme, Haltungsänderungen sowie Reinigungs- und Schlucktechniken (22). Mittels des Einsatzes von Narrow-Band-Imaging (NBI) im Rahmen der FEES lässt sich eine Verbesserung des Kontrastes des Bolus und somit eine erleichterte Auswertung der Untersuchung erreichen (23;24).

Der Untersuchungsablauf sollte, je nach vorangegangener Anamnese und endoskopischem Befund in Ruhe, individuell auf den Patienten abgestimmt und neben verschiedenen Nahrungskonsistenzen sollte ggf. auch das Schluckvermögen von Tabletten überprüft werden (20). Eine Schweregradeinteilung erfolgt häufig an Hand der achtstufigen Penetrations-Aspirations-Skala („1 = Material dringt nicht in die Luftwege ein“ bis „8 = Material dringt in die Luftwege bis unter die Stimmlippen ein, ohne nachweisbare Anstrengung zur Entfernung“) (26).
Bei bestimmten Fragestellungen kann eine videofluoroskopische Evaluation des Schluckaktes (VFSS, kontrastmittelgestützte radiologische Untersuchung) mit Aufzeichnung des gesamten Schluckvorganges (> 25 Bilder/s) sinnvoll sein (12;19).
Kommen differenzialdiagnostisch gastroenterologische Erkrankungen in Betracht (siehe Tabelle 4), sollte eine Ösophagogastroduodenoskopie (ÖGD) mit spezifischer Fragestellung einer ösophagealen Dysphagie (vorsichtiges Eingehen in den Ösophagus und langsames Vorschieben, Stufenbiopsien des Ösophagus, Beurteilung der Peristaltik, Speisereste) durchgeführt werden (22). Ergänzend zur ÖGD kann eine Ösophagusbreischluckuntersuchung sinnvoll sein. Vor allem bei retrosternalen Beschwerden in Kombination mit einer Dysphagie sollten nach Ausschluss anderer Ursachen eine Ösophagusmotilitätsstörung in Betracht gezogen und ggf. eine Ösophagusmanometrie ergänzt werden.

Ziel der Diagnostik sollte eine möglichst genaue Beschreibung des individuellen Störungsmusters des Schluckaktes und noch vorhandener Funktionen des betreffenden Patienten sein, um eine individualisierte Therapiestrategie mit zu entwickeln (27). Ergänzend sollte das Energiedefizit ermittelt werden, das durch therapeutische Maßnahmen ausgeglichen werden muss und die Nahrungskonsistenz, die ein sicheres Schlucken ermöglicht (19).
Therapie
Unterschieden wird in der logopädischen Schlucktherapie zwischen Restitution (komplette oder partielle Wiederherstellung gestörter Schluckabläufe unter Ausnutzung der ZNS-Plastizität durch Stimulation sowie aktivierende und repetitive Übungen ohne Nahrungsangebot), Kompensation (Ausnutzen erhalten gebliebener Funktionen mittels „Schluckmanöver“ und Haltungsänderungen, z. B. supraglottisches Schlucken, Chin-down-Manöver) und Adaptation. Letztere umfasst diätetische Maßnahmen wie Konsistenzänderungen (z. B. Andicken von Flüssigkeiten zur Vermeidung von Flüssigkeitsaspirationen) sowie Ess-/Trinkhilfen (z. B. Nasenausschnittsbecher zur Ermöglichung einer nach unten geneigten Kopfhaltung beim Schlucken) (12;27).
Bei dem adaptiven Verfahren einer Konsistenzmodifikation sollte ein gesteigertes Risiko von Dehydratation und Malnutrition beachtet und nur nach sorgfältiger Evaluation des Schluckaktes empfohlen werden. Es ist eine genaue Definition des Andickungsgrades (nektarartig, sirupartig, honigartig, puddingartig) sinnvoll, damit vor allem Flüssigkeiten nicht zu stark angedickt und somit eine ausreichende Flüssigkeitsaufnahme nicht erschwert wird. In kleineren Studien zeigte sich kein Anstieg der Aspirationspneumonierate bei Einnahme von unangedicktem Wasser zwischen den Mahlzeiten (19;28-32).
Eine bestehende medikamentöse Therapie aufgrund anderer Grunderkrankungen sollte regelmäßig kritisch bezüglich möglicher Nebenwirkungen/Wechselwirkungen im Sinne einer medikamentenassoziierten Dysphagie bzw. Symptomverstärkung einer Presbyphagie, vor allem bei Einnahme multipler Medikamente, geprüft werden (33).
Elektrostimulationsverfahren (z. B. pharyngeale Elektrostimulation, neuromuskuläre Oberflächenstimulation) haben bei Schlaganfallpatienten im Rahmen kleinerer Studien erste Erfolge gezeigt – ob sich diese auch auf Patienten mit Presbydysphagie übertragen lassen, bleibt abzuwarten.
Fazit für die Praxis
Presbydysphagie kann Ursache von Malnutrition, ungewolltem Gewichtsverlust, häufigen bronchopulmonalen Infekten und Aspirationspneumonien, Wirkverlust oral eingenommener Medikation, aber auch von sozialem Rückzug im Alter sein und sollte differenzialdiagnostisch vor allem bei geriatrischen Patienten in Betracht gezogen werden. Es sollte je nach Störungskomponenten eine möglichst individualisierte Schlucktherapie angestrebt werden.
Interessenkonflikte
Ein Interessenkonflikt wird von der Autorin verneint.
Literatur
- Turley R, Cohen S: Impact of voice and swallowing problems in the elderly. Otolaryngol Head Neck Surg 2009; 140: 33-36.
- Lin LC, Wu SC, Chen HS et al.: Prevalence of impaired swallowing in intsitutionalized older people in taiwan. J Am Geriatr Soc 2002; 50: 1118-1123.
- Butler SG, Stuart A, Markley L et al.: Penetration und aspitation in healthy older adults as assessed during endoscopic evaluation of swallowing. Ann Otol Rhinol Laryngol 2009; 118: 190-198.
- Muhle P, Wirth R, Glahn J, Dziewas R: Schluckstörungen im Alter. Physiologie und Pathophysiologie. Nervenarzt 2015; 86: 440-451.
- Serra-Prat M, Palomera M, Gomez C et al.: Oropharyngeal dysphagia as a risk factor for malnutrition and lower respiratory tract infection in independently living older persons: a population-based prospective study. Age Ageing 2012; 41: 376-381.
- Maeda K, Akagi J: Decreased tongue pressure is associated with sarcopenia and sarcopenic dysphagia in the elderly. Dysphagia 2015; 30: 80-87.
- Milosavljevic Z, Zelen I, Tanaskovic I et al.: Morphometric analysis of muscularis proper and myenteric plexus of the normal human oesophagus. Age related changes. Folia Morphol (Warsz) 2013; 72: 223-229.
- Logemann JA, Pauloski BR, Rademaker AW et al.: Temporal and biomechanical characteristics of oropharyngeal swallow in younger and older men. J Speech Lang Hear Res 2000; 43: 1264-1274.
- Allepaerts S, Delcourt S, Petermans J: Swallowing disorders in elderly patients: a multidisciplinary approach. Rev Med Liege 2014; 69: 349-356.
- Jungheim M, Schwemmle C, Miller S, Kühn D, Ptok M: Schlucken und Schluckstörungen im Alter. HNO 2014; 62: 644-651.
- Nienstedt JC, Pflug C: Altersbedingte Dysphagie frühzeitig erkennen. HNO-Nachrichten 2017; 47 (6).
- Prosiegel M: Diagnostik und Therapie neurogener Dysphagie. HNO-Nachrichten 2015; 45 (2).
- Leopold NA, Daniels SK: Supranuclear control of swallowing. Dysphagia 2010; 25: 250-257.
- Ertekin C, Aydogdu I: Neurophysiology of swallowing. Clin Neurophysiol 2003; 114: 2226-2244.
- Jean A: Brain stem control of swallowing: neuronal network and cellular mechanisms. Physiol Rev 2001; 81: 929-969.
- Shaw SM, Martino R: The normal swallow: muscular and neurophysiological control. Otolaryngol Clin North Am 2013; 46: 937-956.
- Namasivayam-MacDonald AM, Barbon CEA, Steele CM: A review of swallow timing in the elderly. Physiology and Behavior 2018;184: 12-26.
- Omari TI, Kritas S, Cock C et al.: Swallowing dysfunction in healthy older people using pharyngeal pressure-flow analysis. Neurogastroenterol Motil 2014; 26: 59-68.
- Wirth R, Dziewas R: Neurogene Dysphagie. Internist 2017; 58: 132-140.
- Nienstedt JC, Pflug C, Flügel T: Effiziente Schluckdiagnostik in der Praxis. HNO-Nachrichten 2018; 48 (3).
- Michaelis S: Gastroenterologische Leitsymptome und Behandlung: Dysphagie. In: Layer P, Rosien U (Hrsg.). Facharztwissen Gastroenterologie, 1. Aufl.; München: Elsevier Urban & Fischer, 2017; 1-3.
- Ott R, Bajbouj M, Feussner H et al.: Dysphagie sicher einordnen, Versorgung koordinieren. MMW-Fortschr Med 2014; 156 (7).
- Nienstedt JC, Müller F, Nießen A et al.: Narrow Band Imaging enhances the detection rate of penetration and aspiration in FEES. Dysphagia 2017; 32: 443-448.
- Fleischer S, Hess M: Verbesserte Schluckdiagnostik mit Narrow Band Imaging. HNO-Nachrichten 2017; 47 (1).
- Langmore SE, Schatz K, Olsen N: Fiberoptic endoscopic examination of swallowing safety: a new procedure. Dysphagia 1988; 2: 216-219.
- Rosenbek JC, Robbins JA, Roecker EB, Coyle JL, Wood JL: A penetration-aspiration scale. Dysphagia 1996; 11: 93-98.
- Di Pede C, Mantovani ME, Del Felice A, Masiero S: Dysphagia in the elderly: focus on rehabilitation strategies. Aging Clin Exp Res 2016; 28: 607-617.
- Arens C, Herrmann IF, Rohrbach S et al.: Positionspapier der DGHNO und der DGPP – Stand der klinischen und endoskopischen Diagnostik, Evaluation und Therapien von Schluckstörungen bei Kindern und Erwachsenen. Laryngo-Rhino-Otol 2015; 94: 306-354.
- Wirth R, Lueg G, Dziewas R: Oropharyngeale Dysphagie im Alter – Abklärung und Therapieoptionen. Dtsch Med Wochenschr 2018; 143: 148-151.
- Ney, DM, Weiss JM, Kind AJH, Robbins J: Senescent swallowing: impact, strategies and interventions. Nutr Clin Pract 2009; 24: 395-413.
- Frey KL, Ramsberger G: Comparsion of outcomes before and after implementation of a water protocol for patients with cerebrovascular accident and dysphagia. J Neurosci Nurs 2011; 43: 165-171.
- Gillman A, Winkler R, Taylor NF: Implementing the Free Water Protocol does not result in aspiration pneumonia in carefully selected patients with dysphagia: a systematic review. Dysphagia 2017; 32: 345-361.
- Schwemmle C, Jungheim M, Miller S et al.: Medikamenteninduzierte Dysphagien. HNO 2015; 63: 504-510.
vorab online
Dieser Artikel wurde am 31. Juli 2019 vorab online veröffentlicht.
