Progrediente interstitielle Lungenerkrankung unter Abirateron (Zytiga®) (Aus der UAW-Datenbank)
Deutsches Ärzteblatt, Jg. 113, Heft 3, 22.01.2016
Informationen zur Wirkungsweise und Indikation von Abirateron
Androgensensitive Prostatakarzinome sprechen auf eine Senkung des Androgenspiegels an. Jedoch wird durch eine Therapie mit Gonadorelin(Gonadotropin-Releasing-Hormon, GnRH)-Agonisten oder -Antagonisten oder bilaterale Orchiektomie nur die Androgenproduktion in den Hoden gehemmt, nicht aber im Tumor selbst und in den Nebennieren. Abirateron hemmt das Enzym CYP17, das in Hoden, Nebennieren und im Prostatatumorgewebe exprimiert wird und für die Androgenbiosynthese erforderlich ist (1). Die Hemmung von CYP17 führt aber auch zu einer erhöhten Mineralokortikoidproduktion in den Nebennieren, die eine Hypertonie, Hypokaliämie und eine Flüssigkeitsretention hervorrufen kann. Abirateron wird daher in Kombination mit Prednison oder Prednisolon angewendet. Durch die so herbeigeführte Suppression der Ausschüttung von adrenokortikotropem Hormon (ACTH) soll die Häufigkeit und Schwere der Nebenwirkungen durch Mineralokortikoide vermindert werden.
Abirateron ist zugelassen zur Behandlung des metastasierten kastrationsresistenten Prostatakarzinoms, wenn die Erkrankung während oder nach einer Docetaxel-haltigen Chemotherapie progredient ist (1). Die Nutzenbewertung durch den Gemeinsamen Bundesausschuss hat für diese Indikation einen Hinweis auf einen beträchtlichen Zusatznutzen ergeben (2). Seit Anfang 2013 ist Abirateron ebenfalls zugelassen bei asymptomatischem oder mild symptomatischem Verlauf, wenn eine Androgenentzugstherapie versagt hat und eine Chemotherapie klinisch noch nicht indiziert ist. Die Verordnungszahlen sind seit 2012 deutlich angestiegen und lagen 2014 bei 1,8 Mio. definierten Tagesdosen (DDD) (3).
Der AkdÄ wurde der Fall eines 70-jährigen Patienten mit einem PSA-progredienten, lokal fortgeschrittenen Prostatakarzinom mit Knochen- und Lymphknotenmetastasen berichtet. Nach Erstdiagnose im Jahr 2005 (initiales Stadium cT1c) wurde eine palliative Strahlentherapie von Th 9–11 mit 30 Gy durchgeführt und nach prophylaktischer Mamillenbestrahlung mit 12 Gy eine Androgendeprivation eingeleitet. Etwa 18 Monate vor der aktuellen stationären Aufnahme war eine medikamentöse Therapie mit Abirateron und Prednisolon begonnen worden. Hierunter entwickelte der Patient einen Hyperaldosteronismus und einen Steroid-Diabetes. Zur stationären Aufnahme führten dann eine zunehmende Belastungsdyspnoe und ein entgleister Diabetes mit Blutzuckerwerten bis 700 mg/dl. Bei Aufnahme lag die Sauerstoffsättigung unter Raumluft bei 85 %. Eine Lungenfunktion erbrachte den Befund einer schwer eingeschränkten CO-Diffusion bei einer kombinierten obstruktiven und restriktiven Ventilationsstörung mit überwiegender Restriktion. Im Röntgen-Thorax zeigte sich eine milchglasartige, diffuse Transparenzminderung des Lungenparenchyms. Diese war im CT beidseitig symmetrisch verteilt, zentral und apikal betont unter Aussparung des Lungenmantels (siehe Abbildung). Differenzialdiagnostisch wurden eine Hypersensitivitätspneumonitis sowie eine eosinophile oder atypische Pneumonie diskutiert. Bronchoskopisch war eine leichte Bronchitis auffällig ohne Anhalt für Malignität in Gewebeproben. In der bronchoalveolären Lavage (BAL) zeigten sich eine deutliche Lymphozytose mit normalem CD4/CD8-Quotienten sowie eine Vermehrung neutrophiler Granulozyten. Laborchemisch waren die Leukozyten normwertig, jedoch fand sich eine Linksverschiebung und das CRP war erhöht. Zunächst wurde eine kalkulierte Antibiotikatherapie mit Cefuroxim und Clarithromycin begonnen. Alle mikrobiologischen Untersuchungen blieben negativ. Die pulmonalen Veränderungen im CT waren jedoch progredient und die klinische Situation verschlechterte sich weiter, sodass eine nichtinvasive Beatmung mittels Nasen-Gesichtsmaske (nCPAP) notwendig wurde. Das antibiotische Regime wurde daher umgestellt auf Piperacillin/Tazobactam und hochdosiertes Cotrimoxazol, letzteres unter dem Verdacht auf eine Pneumonie durch Pneumocystis jiroveci. Nach Ausschluss einer Infektion mit CMV, Legionellen, Influenza, Mycoplasmen, Chlamydien sowie einer Tuberkulose und Pneumocystis wurde Abirateron als möglicher Auslöser der interstitiellen Lungenerkrankung pausiert und eine Stoßtherapie mit 500 mg Prednisolon täglich für drei Tage begonnen. Hierunter besserte sich die klinische Symptomatik, die nichtinvasive Beatmung konnte beendet werden und es erfolgte in bereits gebessertem Zustand eine Verlegung in eine pneumologische Klinik. Die dort durchgeführten Untersuchungen bzgl. einer etwaigen exogen-allergischen Alveolitis oder einer Erkrankung aus dem rheumatischen Formenkreis waren nicht wegweisend, sodass der Verdacht auf eine medikamentös induzierte Alveolitis bestehen blieb.
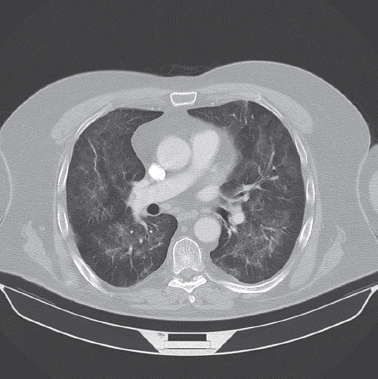
Abbildung 1: Thorakale Computertomographie mit geographisch verteilter, milchglasartiger Transparenzminderung des Lungenparenchyms
Bei dem Patienten im dargestellten Fall wurde die Verdachtsdiagnose einer Alveolitis auf dem Boden einer medikamenten-toxischen Wirkung von Abirateron gestellt. In Deutschland gibt es zu Abirateron aktuell keine ähnlichen Verdachtsfälle. In der Datenbank der Europäischen Arzneimittel-Agentur sind bis Mai 2015 insgesamt 2293 Verdachtsberichte über unerwünschte Arzneimittelwirkungen von Abirateron erfasst: In etwa 200 Fällen wird über Erkrankungen der Atemwege, des Brustraums und des Mediastinums berichtet. Eine interstitielle Lungenerkrankung wird 14-mal genannt.
Medikamenten-induzierte interstitielle Lungenerkrankungen
Medikamenten-induzierte Schäden können alle Abschnitte der Lunge betreffen, am häufigsten ist jedoch das Lungenparenchym beteiligt (4). Der Fibrosierung der Lunge geht in der Regel eine akute oder subakut verlaufende Alveolitis – wie in unserem Fall beschrieben – voraus, die potenziell reversibel ist. Aus diesem Grund ist das Erkennen des Frühstadiums von besonderer Bedeutung. Die Diagnose einer medikamenten-induzierten Alveolitis mit der Gefahr der Entwicklung einer interstitiellen Lungenerkrankung (engl. drug-induced interstitial lung disease, DILD) kann schwierig sein, da die klinischen Befunde wie Husten, Fieber, Dyspnoe und Hypoxämie unspezifisch sind. Eine Alveolitis und DILD sollten in Betracht gezogen werden, wenn die genannten klinischen Symptome und passende Befunde in der Bildgebung auftreten, ohne dass es Hinweise auf eine dekompensierte Herzinsuffizienz oder eine ursächliche Infektions- oder Tumorerkrankung gibt (5). In vielen Fällen handelt es sich um eine Ausschlussdiagnose. Zahlreiche Medikamente werden mit dem Auslösen einer Alveolitis und nachfolgender DILD in Zusammenhang gebracht, wie z. B. Minocyclin, Methotrexat (MTX), Nitrofurantoin, Amiodaron oder Bleomycin (ausführliche Liste unter: www.pneumotox.com). Eine Besserung der Symptomatik nach Absetzen des als ursächlich betrachteten Arzneimittels erhärtet den Verdacht.
Bei der Bildgebung steht die hochauflösende Computertomographie (HRCT) im Vordergrund; die Befunde entsprechen jedoch denen einer Alveolitis und bei weiter fortgeschrittenen Erkrankungen denen bei interstitiellen Lungenerkrankungen anderer Ursache. Auch die histologischen Befunde können unspezifisch sein. Ein häufiger Befund in der bronchoalveolären Lavage (BAL) ist eine lymphozytäre Alveolitis mit einem Überwiegen der CD8-Zellen. Die Lungenfunktion zeigt eine restriktive Ventilationsstörung mit Erniedrigung der totalen Lungenkapazität (TLC) in der Bodyplethysmographie, verminderter Vitalkapazität (VC) in der Spirometrie und einer geringeren Diffusionskapazität für CO (DLCO) als Ausdruck der gestörten Permeabilität der alveolokapillären Membran.
Zusammenfassung und Empfehlung der AkdÄ
Zahlreiche Medikamente werden mit dem Auslösen einer Alveolitis und nachfolgender interstitieller Lungenerkrankung (engl. drug-induced interstitial lung disease, DILD) in Zusammenhang gebracht. Eine DILD sollte in Betracht gezogen werden, wenn Husten, Fieber, Dyspnoe und Hypoxämie in Verbindung mit dem Befund einer interstitiellen Lungenerkrankung in der Bildgebung auftreten, ohne dass es Hinweise auf eine dekompensierte Herzinsuffizienz oder eine ursächliche Infektions- oder Tumorerkrankung gibt. Therapeutisch empfiehlt sich vor allem das Absetzen des als ursächlich angesehenen Arzneimittels sowie in einigen Fällen die Gabe von Glukokortikosteroiden.
Der AkdÄ wurde der Fall einer DILD im Zusammenhang mit Abirateron (Zytiga®) gemeldet. Weitere Verdachtsberichte sind in der europäischen Nebenwirkungsdatenbank erfasst. Ob wirklich ein kausaler Zusammenhang vorliegt, kann anhand dieser Daten nicht abschließend beurteilt werden. Bei einer entsprechenden Symptomatik unter laufender Therapie mit Abirateron sollte jedoch die Differenzialdiagnose einer DILD einbezogen und Verdachtsfälle der AkdÄ mitgeteilt werden.
Literatur
- Janssen-Cilag International NV: Fachinformation „Zytiga® 250 mg Tabletten“. Stand: November 2014.
- Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII – Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach § 35a des Fünften Buches Sozialgesetzbuch (SGB V) – Abirateronacetat. 29. März 2012. Dtsch Arztebl 2012; 109: A 1392–1394.
- Schwabe U, Paffrath D (Hrsg.): Arzneiverordnungs-Report 2015. Berlin, Heidelberg: Springer-Verlag, 2015.
- Prasad R, Gupta P, Singh A, Goel N: Drug induced pulmonary parenchymal disease. Drug Discov Ther 2014; 8: 232–237.
- Matsuno O: Drug-induced interstitial lung disease: mechanisms and best diagnostic approaches. Respir Res 2012; 13: 39.
