„UAW-News International“: Anwendungsbeschränkung von Fluorchinolonen
Rubrik: Bekanntgaben DÄB
Nachdruck aus: Deutsches Ärzteblatt 2023; 120: A 1700-1701
Chinolon- und Fluorchinolon-haltige Antibiotika werden seit vielen Jahren zur Behandlung bakterieller Infektionen eingesetzt. Während die früher angewendeten Chinolone ein enges Wirkspektrum gegen Gram-negative Erreger besaßen, sind die neueren Fluorchinolone breiter wirksam (1). In Deutschland sind aktuell die Fluorchinolone Ciprofloxacin, Delafloxacin, Levofloxacin, Moxifloxacin, Norfloxacin und Ofloxacin zugelassen (2), wobei Delafloxacin noch nicht auf dem Markt erhältlich ist. Das am häufigsten zu Lasten der gesetzlichen Krankenversicherung verordnete Fluorchinolon ist Ciprofloxacin mit über 7 Millionen definierten Tagesdosen im Jahr 2021 (3).
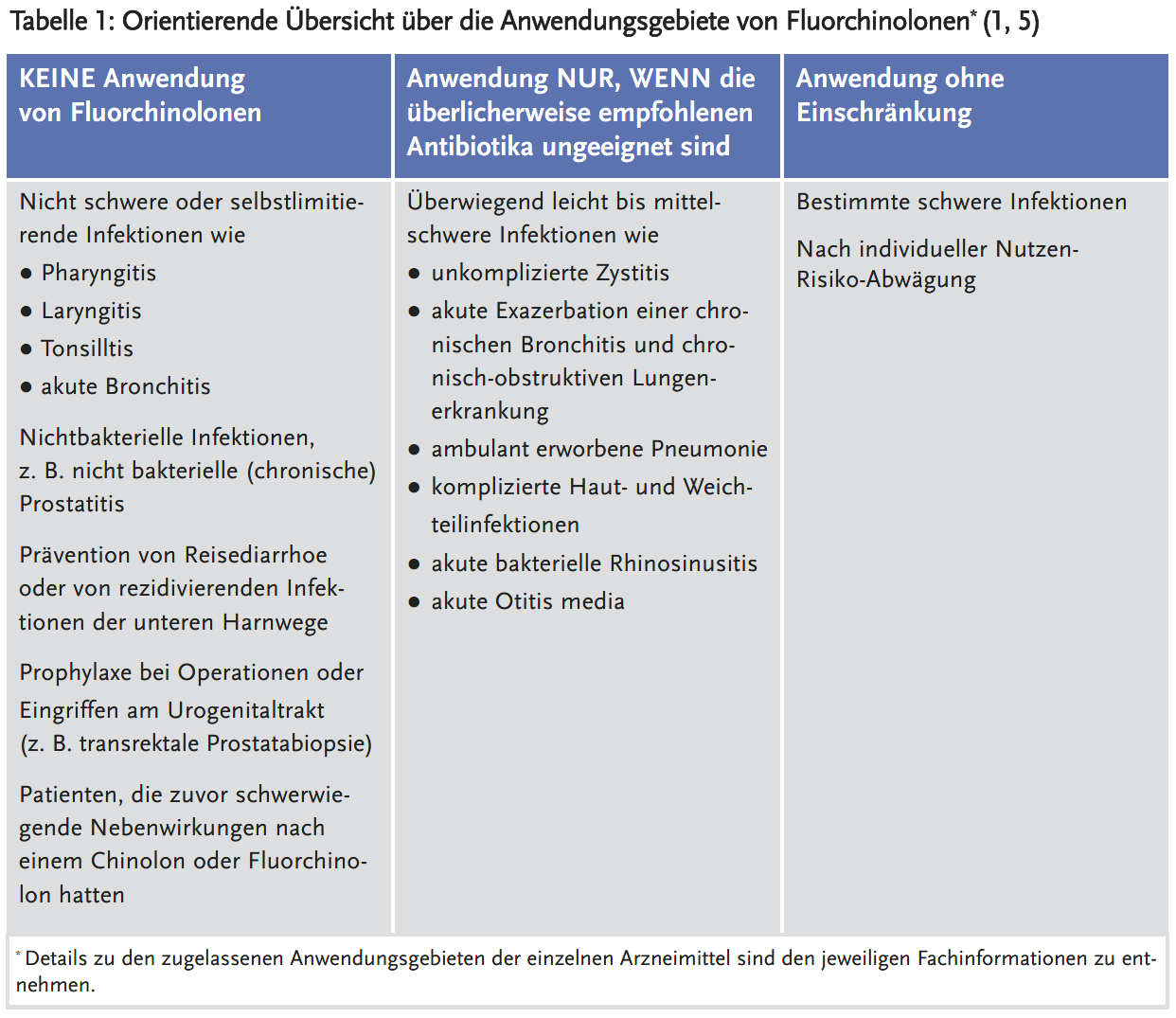
Auf Initiative des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM) überprüfte der Ausschuss für Risikobewertung im Bereich der Pharmakovigilanz (PRAC) der Europäischen Arzneimittel-Agentur (EMA) 2017–2018 im Rahmen eines Risikobewertungsverfahrens in der gesamten EU das Risiko für sehr seltene, jedoch langanhaltende, die Lebensqualität beeinträchtigende und möglicherweise irreversible Nebenwirkungen im Zusammenhang mit systemisch wirkenden (systemische und inhalative Anwendung) Fluorchinolonen (2). Adressiert wurden hauptsächlich muskuloskelettale und neuropsychiatrische Reaktionen (wie Tendinitis, Sehnenruptur, Arthralgie, Gangstörung, Neuropathie, Depression, Fatigue, Gedächtnisstörungen, Schlafstörungen sowie Beeinträchtigungen von Hören, Sehen, Riechen und Schmecken). Diese können bereits während der Anwendung, aber auch mit einer Zeitverzögerung von einigen Monaten auftreten (4, 5). Für das Verfahren wertete der PRAC nicht nur klinische und nichtklinische Studiendaten aus, sondern auch Spontanmeldungen und wissenschaftliche Literatur (1). Im Ergebnis wurde die Anwendung von Fluorchinolon-haltigen Arzneimitteln deutlich eingeschränkt (siehe Kasten 1): Einige Indikationen, für die das Nutzen-Risiko-Verhältnis nun als negativ bewertet wird, wurden komplett gestrichen. Dazu gehören beispielsweise Pharyngitis und Tonsillitis, da diese nicht schweren Erkrankungen zumeist viral bedingt sind und für bakterielle Formen besser geeignete Antibiotika zur Verfügung stehen. Bei einigen anderen bakteriellen Infektionen sollten Fluorchinolone nur angewendet werden, wenn die üblicherweise verwendeten Antibiotika nicht geeignet sind. Hierzu zählen unter anderem unkomplizierte Zystitis und akute bakterielle Rhinosinusitis. Ohne Einschränkungen des Anwendungsgebiets blieben bestimmte schwere Infektionen oder Infektionen mit möglicherweise schwerwiegenden Komplikationen wie komplizierte Harnwegsinfektionen und Pyelonephritis bestehen (siehe Tabelle 1) (1). Im April 2019 wurden die Angehörigen der Heilberufe in einem ersten Rote-Hand-Brief hierüber informiert (4).

Seither wurde eine von der EMA finanzierte Arzneimittelanwendungsstudie (study of impact of EU label changes for fluoroquinolone containing medicinal products for systemic and inhalation use – post-referral prescribing trends) zu systemisch wirkenden Fluorchinolonen durchgeführt (6). Dazu wurden ambulante Verordnungen von Fluorchinolonen aus den Jahren 2016 bis 2021 aus Belgien, Deutschland, Frankreich, den Niederlanden, Spanien und dem Vereinigten Königreich ausgewertet. Die Häufigkeit der Verschreibung schwankte in allen Kalenderjahren und lag zwischen 0,7 (minimaler Wert in Großbritannien) und 8,0 Verordnungen (maximaler Wert in Spanien) pro 1000 Personen pro Monat. Am häufigsten wurden Fluorchinolone bei Menschen über 75 Jahren verordnet. Die Indikation für die Fluorchinolon-Behandlung war in den Daten häufig nicht ersichtlich. Wenn jedoch die Indikation abgeleitet werden konnte, dann waren die häufigsten Indikationen Atemwegs-, unkomplizierte Harnwegs- sowie Ohrinfektionen. Außer in Großbritannien war der Anteil der Off-label-Verordnungen höher als der Anteil der In-label-Verordnungen. Während des Studienzeitraums wurde eine Abnahme der Fluorchinolon-Verordnungen in Deutschland beobachtet. Da dieser Trend allerdings schon vor der Änderung der Fachinformation und dem Rote-Hand-Brief in 2019 begonnen hat, kann er nicht allein auf die regulatorischen Maßnahmen zurückgeführt werden (2, 6).
Der PRAC befasste sich angesichts dieser Daten erneut mit dem Risiko langanhaltender, die Lebensqualität beeinträchtigender, schwerwiegender Nebenwirkungen von systemisch wirkenden Fluorchinolonen. Seiner Empfehlung folgend wurde im Juni dieses Jahres ein neuerlicher Rote-Hand-Brief versendet, um an die Anwendungsbeschränkungen zu erinnern (siehe Kasten 1) (5).
Im Rahmen des oben erwähnten EU-weiten Risikobewertungsverfahrens wurden keine aussagekräftigen Fallberichte zu schwerwiegenden Nebenwirkungen im Zusammenhang mit lokal angewendeten Fluorchinolonen identifiziert. Die Anwendung von Fluorchinolon-haltigen Arzneimitteln an Augen und Ohren sollte jedoch vermieden werden, wenn zuvor schwere und insbesondere anhaltende Nebenwirkungen nach systemischer oder inhalativer Anwendung aufgetreten sind (7).
Im aktuellen Rote-Hand-Brief wird noch an zwei weitere Risiken im Zusammenhang mit Fluorchinolonen erinnert, nämlich das Risiko von Aortenaneurysmen und -dissektionen sowie das Risiko von Herzklappenregurgitation und -insuffizienz (5). Bei Patienten mit Risikofaktoren für diese Erkrankungen, sollten Fluorchinolone mit systemischer Wirkung nur nach sorgfältiger Nutzen-Risiko-Abwägung verordnet werden (8, 9).
Fazit
Trotz der Anwendungsbeschränkungen werden systemisch wirkende Fluorchinolone auch in Deutschland weiterhin außerhalb der empfohlenen Anwendungsgebiete angewendet. Aufgrund des Risikos für teilweise langanhaltende, die Lebensqualität beeinträchtigende und möglicherweise irreversible Nebenwirkungen soll nochmals erinnert werden, dass sie nur in den zugelassenen Indikationen und nur nach sorgfältiger Nutzen-Risiko-Abwägung verordnet werden sollen. Zu beachten ist, dass in vielen Indikationen Fluorchinolone nur als Mittel der letzten Wahl angewendet werden sollen (siehe Tabelle 1). Patienten sollten über die Risiken aufgeklärt und aufgefordert werden, bei den ersten Anzeichen für derartige Nebenwirkungen die Behandlung zu pausieren und ärztlichen Rat einzuholen. Besondere Vorsicht ist geboten bei Älteren, Niereninsuffizienz, gleichzeitiger Kortikosteroidbehandlung und nach Organtransplantation.
Literatur
- European Medicines Agency. Assessment report: Referral under Article 31 of Directive 2001/83/EC resulting from pharmacovigilance data: Quinolone and fluoroquinolone medicinal products for systemic and inhalation use; EMA/818158/2018. London; 16.10.2018. Verfügbar unter: https://www.ema.europa.eu/en/documents/referral/quinolone-fluoroquinolone-article-31-referral-assessment-report_en.pdf.
- Ortiz de Orué Lucana D, Grüger T, Lee SM, Lex D, Huber M. Zehn Jahre PRAC – der Ausschuss für Risikobewertung im Bereich der Pharmakovigilanz. Bulletin für Arzneimittelsicherheit 2023; (2):30–8.
- Kern WV. Bakterielle und virale Infektionserkrankungen und Mykosen. In: Ludwig W-D, Mühlbauer B, Seifert R, Hrsg. Arzneiverordnungs-Report 2022. Berlin: Springer-Verlag; 2022. S. 361–83.
- Zulassungsinhaber Fluorchinolon-haltiger Arzneimittel. Systemisch und inhalativ angewendete Chinolon- und Fluorchinolon-Antibiotika: Risiko von die Lebensqualität beeinträchtigenden, lang anhaltenden und möglicherweise irreversiblen Nebenwirkungen – Anwendungsbeschränkungen; Rote-Hand-Brief; 8.4.2019.
- Zulassungsinhaber Fluorchinolon-haltiger Arzneimittel. Systemisch und inhalativ angewendete Fluorchinolon-haltige Antibiotika – Erinnerung an die Anwendungsbeschränkungen; Rote-Hand-Brief; 7.6.2023.
- Pacurariu A, Flach C, Markov E, Lysen T, Ly N, Layton D. Study of impact of EU label changes for fluoroquinolone containing medicinal products for systemic and inhalation use – post-referral prescribing trends: Final Study Report V 3.0; EMA/430636/2019; 31.3.2022. Verfügbar unter: https://www.encepp.eu/encepp/openAttachment/studyResult/48007.
- Bundesinstitut für Arzneimittel und Medizinprodukte. FAQ zu Fluorchinolon-Antibiotika [Stand: 04.07.2023]. Verfügbar unter: https://www.bfarm.de/DE/Arzneimittel/Pharmakovigilanz/Themendossiers/Fluorchinolone/Fluorchinolone_FAQ.html?nn=594580.
- Zulassungsinhaber Fluorchinolon-haltiger Arzneimittel. Systemisch und inhalativ angewendete Fluorchinolone: Risiko für Aortenaneurysmen und -dissektionen; Rote-Hand-Brief; 26.10.2018.
- Zulassungsinhaber Fluorchinolon-haltiger Arzneimittel. Systemisch und inhalativ angewendete Fluorchinolone: Risiko einer Herzklappenregurgitation/ -insuffizienz; Rote-Hand-Brief; 29.10.2020.
