Difelikefalin (Kapruvia®) ▼ – frühe Nutzenbewertung
Neue Arzneimittel
Dieser Artikel wurde am 24. April 2023 vorab online veröffentlicht.
In Kürze
- Difelikefalin ist zugelassen zur Behandlung erwachsener Hämodialysepatienten mit mäßigem bis schwerem Pruritus im Zusammenhang mit einer chronischen Nierenerkrankung (CKD-aP).
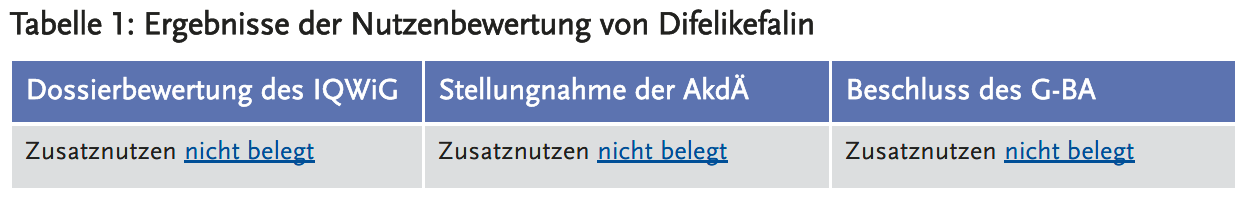
- Nach Einschätzung des IQWiG und der AkdÄ ist der Zusatznutzen nicht belegt.
- Der G-BA folgte dieser Einschätzung und beschloss, dass der Zusatznutzen nicht belegt ist.
Difelikefalin ist ein selektiver κ(Kappa)-Opioidrezeptor-Agonist. Aufgrund seiner hohen Wasserlöslichkeit weist Difelikefalin nur eine geringe ZNS-Gängigkeit auf. Difelikefalin aktiviert in erster Linie periphere κ-Opioidrezeptoren in sensorischen Neuronen, Immunzellen und Keratinozyten der Haut. Hierdurch soll das Gleichgewicht zwischen κ- und µ-Opioidrezeptor-Aktivierung wiederhergestellt werden. Zudem werden antiinflammatorische Effekte diskutiert.
Der Gemeinsame Bundesausschuss (G-BA) legte die folgende Fragestellung fest und definierte dazu die zweckmäßige Vergleichstherapie (ZVT):
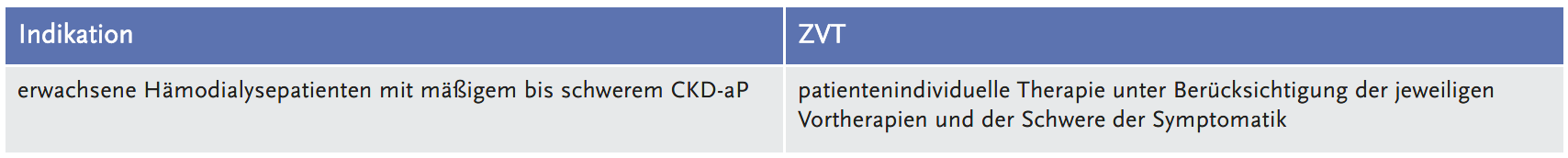
Vorgelegte Evidenz
Vom pharmazeutischen Unternehmer (pU) wurden die randomisierten, kontrollierten Schwesterstudien KALM-1 (1) und KALM-2 (2) vorgelegt. Die Studien schlossen insgesamt 851 Patienten mit terminaler Niereninsuffizienz ein, die trotz adäquater, mindestens dreimal wöchentlicher Hämodialyse unter mäßigem bis schwerem CKD-aP litten. Die Patienten erhielten im Verhältnis 1:1 intravenös Difelikefalin oder Placebo zum Ende jeder Dialyse. Die randomisierte Behandlungsphase dauerte in beiden Studien zwölf Wochen. Die Intensität des Pruritus wurde mittels Worst Itching Intensity Numeric Rating Scale (WI-NRS) erfasst, die von 0 (kein Juckreiz) bis 10 (schlimmstmöglicher Juckreiz) reicht.
Primärer Endpunkt der Studien war der Anteil der Patienten mit einer Verbesserung um ≥ 3 Punkte des wöchentlichen WI-NRS-Durchschnittscores in Woche 12. Der primäre Endpunkt wurde von mehr Patienten unter Difelikefalin erreicht, wobei der Behandlungsunterschied im Vergleich zu Placebo nur in der Studie KALM-1 (43 % vs. 27 %; p < 0,001), nicht aber in der Studie KALM-2 (40 % vs. 30 %; p = 0,092) signifikant war. In der gepoolten Analyse betrug die absolute Risikoreduktion (ARR) 12 %, d. h. jeder neunte Patient profitierte von Difelikefalin hinsichtlich des primären Endpunktes.
In der gepoolten Analyse von KALM-1 und KALM-2 traten unerwünschte Ereignisse (UE) signifikant häufiger unter Difelikefalin auf als unter Placebo (68 % vs. 62 %). Auffällig ist eine numerische Häufung neurologisch-psychiatrischer Erkrankungen unter Difelikefalin (Schwindelgefühle, Somnolenz, Veränderung des Gemüts- und kognitiven Zustands), die nach Einschätzung der europäischen Arzneimittel-Agentur (EMA) am ehesten auf eine zentrale Wirkung von Difelikefalin zurückzuführen ist.
Dossierbewertung des IQWiG
Aus Sicht des IQWiG (3) legt der pU keine geeigneten Studien zur Nutzenbewertung vor:
- Die randomisierte Behandlungsphase in den Studien KALM-1 und KALM-2 ist mit zwölf Wochen zu kurz für das Anwendungsgebiet.
- Die ZVT wurde in den Studien KALM-1 und KALM-2 nicht adäquat umgesetzt, da keine patientenindividuelle Therapie des Pruritus erfolgte.
Stellungnahme der AkdÄ
Die AkdÄ (4) schließt sich der Einschätzung des IQWiG an:
- Der CKD-aP ist eine chronische Erkrankung. Um Wirksamkeit und Risiken einer langfristigen Behandlung abschätzen zu können, sind Studiendaten über eine Dauer von mindestens 52 Wochen erforderlich.
- Mehr als die Hälfte der eingeschlossenen Patienten erhielten zu Studienbeginn keinerlei juckreizstillende Medikation. Sofern überhaupt eine Therapie des CKD-aP erfolgte, so wurden mehrheitlich (80 %) sedierende Antihistaminika eingesetzt, obgleich diese in aktuellen Leitlinien nicht empfohlen werden. (5) Gabapentin und Pregabalin – die erste Wahl bei CKD-aP – wurden kaum genutzt (1,3 % der Patienten). Auch eine Basistherapie mit Emollienzien ist laut den Angaben des pU nur in Einzelfällen erfolgt (< 1 % der Patienten). Im Studienverlauf durften keine neuen Therapien gegen CKD-aP begonnen werden und Dosisanpassungen sollten vermieden werden, obgleich die Behandlung des CKD-aP zu Studienbeginn offensichtlich unzureichend war (durchschnittlicher WI-NRS-Score 7). Zudem waren Therapieoptionen, die als zweite (UVB-Therapie) oder dritte Wahl (Naloxon, Naltrexon) eingestuft werden, generell nicht erlaubt. Zusammenfassend ist es aus Sicht der AkdÄ unklar, ob bei einer adäquaten Umsetzung der Vergleichstherapie (insbesondere Emollienzien und Gabapentin/Pregabalin) ein signifikanter Behandlungsunterschied zwischen Difelikefalin und Placebo bestehen würde.
Beschluss des G-BA
Die Umsetzung der ZVT wird durch den G-BA (6) nicht diskutiert. Nach Einschätzung des G-BA sind die vorgelegten Studien KALM-1 und KALM-2 bereits aufgrund ihrer lediglich zwölfwöchigen randomisierten Studienphase ungeeignet für die frühe Nutzenbewertung einer chronischen Erkrankung. Da keine geeigneten Studiendaten vorgelegt wurden, ist der Zusatznutzen laut Beschluss des G-BA nicht belegt.
Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden.
Literatur
- Fishbane S, Jamal A, Munera C et al.: A phase 3 trial of difelikefalin in hemodialysis patients with pruritus. N Engl J Med 2020; 382: 222-232.
- Topf J, Woolbridge T, McCafferty K et al.: Efficacy of difelikefalin for the treatment of moderate to severe pruritus in hemodialysis patients: pooled analysis of KALM-1 and KALM-2 phase 3 studies. Kidney Med 2022; 4: 100512.
- IQWiG Dossierbewertung: https://www.g-ba.de/downloads/92-975-6140/2022-10-01_Nutzenbewertung-IQWiG_Difelikefalin-D-854.pdf.
- Stellungnahme der AkdÄ: https://www.akdae.de/fileadmin/user_upload/akdae/Stellungnahmen/AMNOG/A-Z/Difelikefalin/Difelikefalin-230123.pdf.
- Stander S, Zeidler C, Augustin M et al.: S2k-Leitlinie: Diagnostik und Therapie des chronischen Pruritus. J Dtsch Dermatol Ges 2022; 20: 1386-1402.
- G-BA: Tragende Gründe: https://www.g-ba.de/downloads/40-268-9411/2023-04-06_AM-RL-XII_Difelikefalin_D-854_TrG.pdf.
