Rebound-Phänomen nach Einnahme von Paxlovid™
Aus der Praxis – für die Praxis
Weitere Autoren: Dr. P.H. Stanislava Dicheva-Radev, Berlin; Prof. Dr. med. Harald Dormann, Erlangen; Dr. med. Dr. Stefan Graafen, Flörsheim
Der Fall
Der AkdÄ wurde ein „Relapse-Phänomen“ nach der Behandlung mit Paxlovid™ gemeldet. Ein 62-jähriger Patient wurde positiv auf SARS-CoV2 (COVID-19) mittels PCR (ct-Wert = 23) getestet und nahm Paxlovid™ für fünf Tage ein. Drei Tage nach Beendigung der medikamentösen Behandlung begann erneut die typische COVID-19-Symptomatik mit Gliederschmerzen, Husten, Schnupfen und Kopfschmerzen. Ein Antigen-Schnelltest fiel positiv aus, sowie eine PCR-Testung (ct-Wert = 21), die sechs Tage nach Ende der Paxlovid™-Gabe durchgeführt wurde.
Die Einnahme von Paxlovid™ wurde korrekt und vollständig wie in der Produktinformation beschrieben durchgeführt. Eine negative PCR-Testung nach der Beendigung der Paxlovid™-Gabe erfolgte nicht, der vom Patienten durchgeführte Schnelltest war zwischenzeitlich negativ.
Das Arzneimittel
Paxlovid™ (150 mg Nirmatrelvir (PF-07321332) + 100 mg Ritonavir Filmtabletten) ist zugelassen zur Behandlung einer Coronavirus-Erkrankung (COVID‑19) bei Erwachsenen, die keine zusätzliche Sauerstoffzufuhr benötigen und ein erhöhtes Risiko haben, einen schweren COVID-19-Verlauf zu entwickeln (1).
Die empfohlene Dosierung beträgt 300 mg Nirmatrelvir und 100 mg Ritonavir zur gleichzeitigen Einnahme alle zwölf Stunden über einen Zeitraum von fünf Tagen.
Die Evidenz
Eine Recherche zu dieser Meldung zeigte, dass es sich nicht um einen Einzelfall handelt. Im Deutschen Ärzteblatt wurde auch über einen solchen Fall berichtet. Hoehl et al. stellten in einem Research Letter den Fall einer Patientin vor, die trotz doppelter Impfung SARS-CoV-2 positiv getestet war und mit Paxlovid™ behandelt wurde. Dabei bildete sich die Symptomatik zunächst zurück und die Patientin wurde negativ getestet. Am zehnten Tag nach der Ersttestung kam es dann unter erneutem Einsetzen von Kältegefühl, Schüttelfrost, Rhinitis, Cephalgie und Diarrhö zu einem erneuten Anstieg der Viruslast mit einem positiven PCR-Test. Die Autoren nehmen an, dass in diesem Fall durch die medikamentöse Senkung der Viruslast eine ausreichende Immunreaktion zur dauerhaften Eliminierung des Virus unterdrückt oder verzögert wurde. Das Auslassen der letzten Paxlovid™-Dosis aufgrund starker Nebenwirkungen könne dies begünstigt haben (2).
Prominentester Paxlovid™-Patient, der ein Rebound-Phänomen im Sommer 2022 erlitt, war der amtierende amerikanische Präsident Joe Biden. Auch er wurde mit Paxlovid™ behandelt, war zwischenzeitlich negativ getestet und durfte seine Quarantäne beenden. Einige Tage später bekam er erneut Husten und wurde wieder positiv getestet (3).
Die amerikanischen Centers for Disease Control and Prevention (CDC) warnten bereits im Mai 2022 in einem Health Advisory, dass nach der Gabe von Paxlovid™ ein COVID-19-Rebound beobachtet wurde, der etwa zwei bis acht Tage nach der initialen Genesung (negativer Test) auftrat und sich durch das erneute Auftreten von COVID-19-Symptomen oder einer erneuten positiven Testung auf COVID-19 auszeichnete (4). Unter den Betroffenen waren auch geimpfte und geboosterte Patienten. Alle hatten laut CDC einen leichten Krankheitsverlauf. Sowohl die Symptome als auch die positiven Testergebnisse besserten sich oder verschwanden (im Median nach drei Tagen) ohne zusätzliche Anti-COVID-19-Behandlung. Die CDC gingen davon aus, dass der COVID-19-Rebound nicht auf eine Reinfektion mit SARS-CoV-2 oder die Entwicklung einer Resistenz gegen Paxlovid™ zurückzuführen war; außerdem wurden bei den bekannten Fällen keine anderen Erreger von Atemwegsinfektionen festgestellt.
Bereits in der klinischen Zulassungsstudie zu Paxlovid™ wiesen 1–2 % der Patienten nach Abschluss der Behandlung ein oder mehrere positive PCR-Testergebnisse auf, nachdem sie zuvor negativ getestet worden waren. Allerdings waren davon auch Patienten aus dem Placebo-Arm betroffen, sodass dies nicht allein auf die Gabe von Paxlovid™ zurückgeführt wurde. Insbesondere weil bei diesen Patienten weder Hospitalisierungen noch Todesfälle vermehrt auftraten. Zudem gab es keine Hinweise darauf, dass der Rebound aufgrund der Entwicklung von Resistenzen gegen Paxlovid™ auftrat (5). Laut FDA gab es zu diesem Zeitpunkt keine Belege für den Nutzen einer längeren Behandlung mit Paxlovid™ (z. B. zehn Tage statt der empfohlenen fünf Tage) oder der Wiederholung einer Behandlung mit Paxlovid™ bei Patienten mit wiederkehrenden COVID-19-Symptomen nach Abschluss einer Behandlung (5).
Im Juni 2022 empfahl das Center for Drug Evaluation and Research (CDER) der FDA allerdings, dass die Fachinformation zu Paxlovid™ bezüglich des viralen RNA-Rebound in der pivotalen Studie EPIC-HR aktualisiert wird. Da Berichte über solche Fälle von COVID-19-Rebounds großes mediales Interesse erweckt hatten, sollten die Ergebnisse der Analysen der Abstrichproben in der EPIC-HR-Studie dargestellt werden, um die Fachkreise besser zu informieren. Diese Analysen der SARS-CoV-2-RNA-Spiegel nach Beendigung der Behandlung wurden in beiden Armen der Studie sowohl vom Sponsor als auch von der FDA unabhängig voneinander durchgeführt (siehe Kasten).
Text der US-amerikanischen Fachinformation (Fact sheet for healthcare providers: interim authorization of Paxlovid™, Stand: 3. November 2022) (7)
Viraler RNA-Rebound
Nach der Behandlung wurden bei einer Subgruppe von Patienten, die Paxlovid™ bzw. Placebo bekommen haben, am Tag 10 und/oder Tag 14 erhöhte SARS-CoV-2-RNA-Ausscheidungsmengen (im Sinne eines Rebounds der viralen RNA) in den nasopharyngealen Proben beobachtet, unabhängig von den COVID-19-Symptomen. Die Häufigkeit des RNA-Rebounds variierte je nach Definition der Analyseparameter, war aber im Allgemeinen vergleichbar in beiden Studienarmen (Paxlovid™ oder Placebo), unabhängig von der verwendeten Rebound-Definition. Im Placebo-Arm war die Inzidenz des RNA-Rebounds im Vergleich zum Paxlovid™-Arm ähnlich oder etwas geringer zu allen Studienzeitpunkten, sowohl während als auch nach der Behandlung.
Der virale RNA-Rebound war nicht mit dem primären klinischen Endpunkt der Studien – COVID-19-bedingte Hospitalisierung oder Tod jeglicher Ursache – bis zum Tag 28 nach Beginn der Behandlung assoziiert. Auch war er nicht mit einer Resistenz gegenüber der Behandlung assoziiert, wie die Sequenzierung der SARS-CoV-2-Hauptprotease zeigte. Die klinische Relevanz des Anstiegs der viralen RNA nach der Behandlung mit Paxlovid™ oder Placebo ist derzeit unklar.
In einem im Juni in JAMA erschienenen Artikel werden weitere Fälle beschrieben und die möglichen Ursachen eines Rebounds diskutiert unter der Prämisse: „Is it the drug, or is it the disease?“ (8). Als ein Beispiel, das dagegenspricht, dass der Rebound Teil des natürlichen Infektionszyklus von COVID-19 sein könnte, wird die Erfahrung der National Basketball Association (NBA) aufgeführt, die täglich ihr komplettes Personal testet. Vom 14. Dezember 2021 bis zum 1. März 2022 – ein Zeitraum, in dem die Omicron-Variante vorherrschend war – gab es Rebounds nur bei den Basketballspielern, nicht aber unter den fast 1000 NBA-Mitarbeitern, die mit COVID-19 diagnostiziert wurden, aber im Gegensatz zu den Spielern nicht mit Nirmatrelvir/Ritonavir behandelt wurden (8).
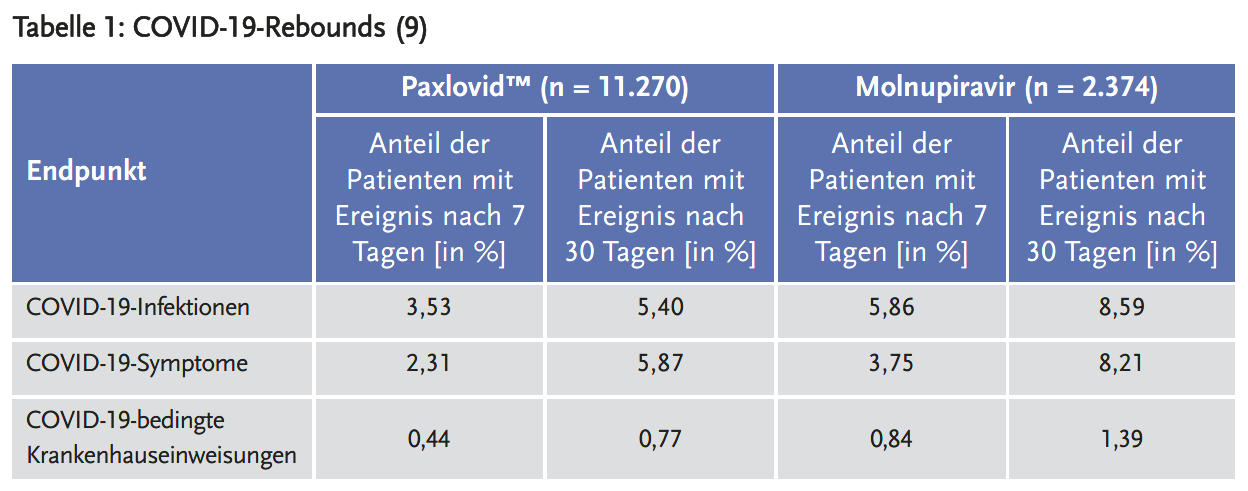
In einer retrospektiven, nicht „peer reviewed“ Analyse von elektronischen Patientenakten aus den USA (9) wurden 13.644 Patienten (> 18 Jahre) evaluiert, die in der Zeit vom 1. Januar 2022 bis 6. August 2022 mit Paxlovid™ oder Molnupiravir aufgrund einer COVID-19-Infektion behandelt wurden. Untersucht wurden drei Endpunkte eines möglichen Rebounds nach 7 und 30 Tagen: COVID-19-Infektionen, COVID-19-Symptome und COVID-19-bedingte Krankenhauseinweisungen (Tabelle 1). Wurde nach der Krankheitsschwere gematcht, gab es keine signifikanten Unterschiede zwischen den beiden Arzneimitteln. Die Patienten mit Rebound hatten jedoch mehr Risikofaktoren als die ohne Rebound.
Offene Fragen
Derzeit ist noch unklar, ob ein Rebound-Phänomen nach Behandlung einer COVID-19-Erkrankung mit Paxlovid™ signifikant häufiger ist als nach spontanem Verlauf. Folgende Fragen können aktuell nicht abschließend beurteilt werden:
- Ist eine zusätzliche Behandlung mit Paxlovid™ oder anderen Anti-SARS-CoV-2-Therapien in Fällen erforderlich, in denen ein COVID-19-Rebound bei entsprechenden Risikopatienten vermutet wird?
- Ist eine Übertragung der Infektion während des COVID-19-Rebounds möglich?
- Wie sollten sich Patienten nach Beginn der Rebound-Symptome verhalten und wie lange eine Maske tragen?
- Gibt es ein SARS-CoV2-variantenspezifisches Risiko für einen COVID-19-Rebound?
Fazit für die Praxis
Ein COVID-19-Rebound nach Behandlung mit Paxlovid™ ist gekennzeichnet durch ein zeitnahes Wiederauftreten der Symptome und/oder einen neuen positiven Test nach einem negativen Test. Derzeit gibt es keine Berichte über schwere Erkrankungen bei Personen mit COVID-19-Rebound sowie keine Hinweise, dass eine zusätzliche Behandlung gegen COVID-19 bei einem Rebound erforderlich ist. Auf der Grundlage der derzeit verfügbaren Daten wird lediglich die Überwachung der Patienten mit einem Wiederauftreten der Symptome nach Abschluss einer Behandlung mit Paxlovid™ empfohlen.
Bei der Verordnung/Abgabe von Paxlovid™ sollten die Patienten auf die Möglichkeit dieses Phänomens hingewiesen werden, insbesondere wenn sie beruflich mit Risikopatienten zu tun haben (Pflegekräfte etc.). Bei Wiederauftreten von COVID-19-typischen Beschwerden nach Ende der Therapie und erfolgter negativen Testung sollte eine erneute Testung eingeleitet werden.
Fälle von COVID-19-Rebounds nach der Behandlung mit Paxlovid™ sollten der AkdÄ gemeldet werden: https://www.akdae.de/arzneimittelsicherheit/uaw-meldung.
Literatur
- Pfizer Europe MA EEIG: Fachinformation „Paxlovid™ 150 mg + 100 mg Filmtabletten“. Stand: Oktober 2022.
- Hoehl S, Toptan T, Rabenau HF, Ciesek S: The relapse phenomenon in mild COVID treated with nirmatrelvir/ritonavir in an immunocompetent patient. Dtsch Arztebl Int 2022; 119: 619-620.
- Biden continues to test positive for COVID-19 after relapse: https://www.voanews.com/a/biden-continues-to-test-positive-for-covid-19-after-relapse-/6684327.html (letzter Zugriff: 8. Dezember 2022). VOA News vom 2. Auguat 2022.
- COVID-19 rebound after paxlovid treatment: https://emergency.cdc.gov/han/2022/han00467.asp (letzter Zugriff: 8. Dezember 2022). CDC Health Alert Network, 24. Mai 2022.
- FDA updates on paxlovid for health care providers: https://www.fda.gov/drugs/news-events-human-drugs/fda-updates-paxlovid-health-care-providers (letzter Zugriff: 8. Dezember 2022). FDA, 4. Mai 2022.
- Emergency Use Authorization (EUA) for Paxlovid. Center for Drug Evaluation and Research Review Memorandum: https://www.fda.gov/media/161018/download (letzter Zugriff: 8. Dezember 2022). CDER – FDA, 5. August 2022.
- Pfizer Private Limited: Fact sheet for healthcare providers: interim authorization of Paxlovid™: https://labeling.pfizer.com/ShowLabeling.aspx?id=16664 (letzter Zugriff: 8. Dezember 2022). Stand: 3. November 2022.
- Rubin R: From positive to negative to positive again – the mystery of why COVID-19 rebounds in some patients who take Paxlovid. JAMA 2022; 327; 24: 2380-2382.
- Wang L, Berger NA, Davis PB et al.: COVID-19 rebound after Paxlovid and molnupiravir during January-June 2022. medRxiv 2022; 2022.06.21.22276724.
Interessenkonflikte
Die Autoren geben an, keine Interessenkonflikte zu haben.
