Cariprazin (Reagila®) (frühe Nutzenbewertung)
In Kürze
- Cariprazin ist zur Behandlung von Schizophrenie zugelassen.
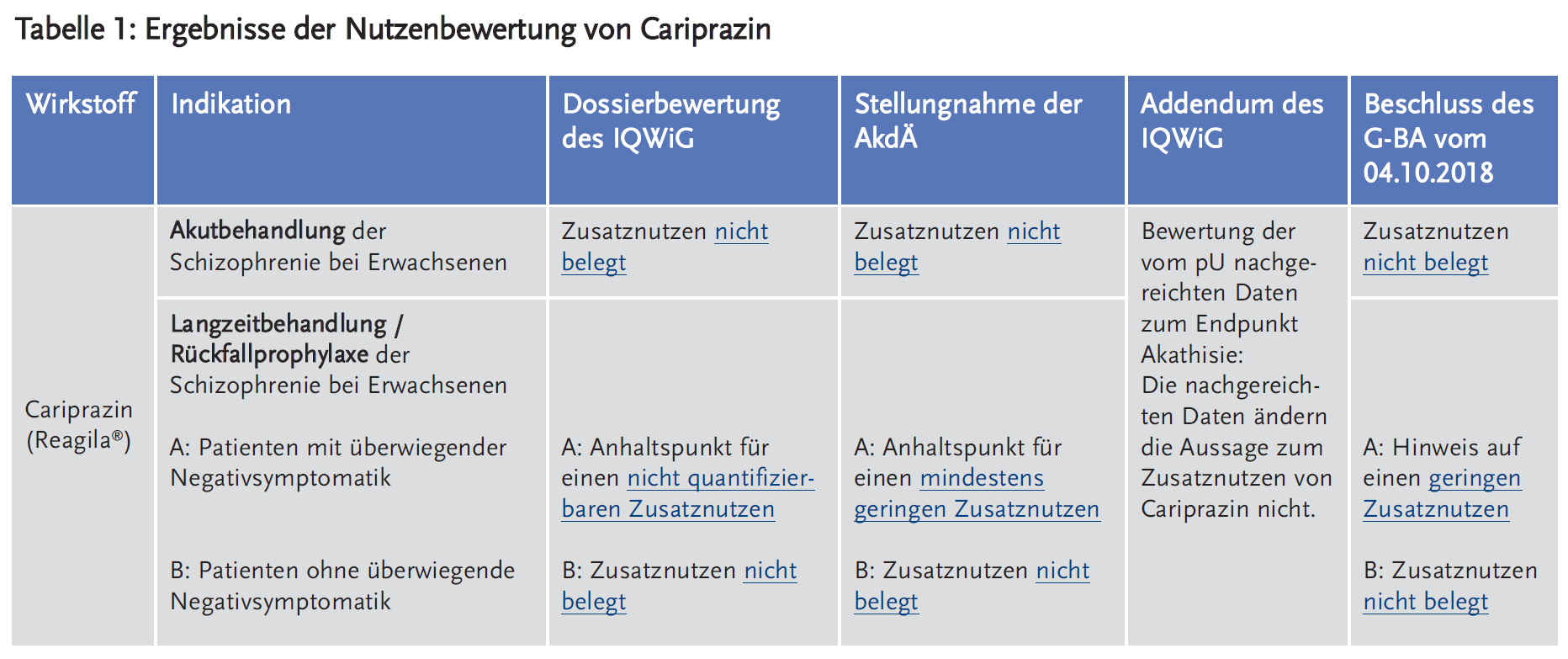
- Das IQWiG bewertete den Zusatznutzen in der Akutbehandlung bei Erwachsenen als nicht belegt, da die zwei vorgelegten Studien aufgrund der fehlenden Möglichkeit einer Dosisanpassung für eine Nutzenbewertung nicht geeignet waren. Die AkdÄ schloss sich dieser Bewertung an.
- In der Langzeitbehandlung/Rückfallprophylaxe bei Erwachsenen lagen nur für die Population der Patienten mit überwiegender Negativsymptomatik verwertbare Daten vor. Für diese Patientenpopulation sah das IQWiG einen Anhaltspunkt für einen nicht quantifizierbaren Zusatznutzen. Die AkdÄ sah einen Anhaltspunkt für einen mindestens geringen Zusatznutzen.
- Der G-BA beschloss, dass der Zusatznutzen in der Akutbehandlung nicht belegt ist. In der Langzeitbehandlung/Rückfallprophylaxe besteht bei Patienten mit überwiegender Negativsymptomatik ein Hinweis auf einen geringen Zusatznutzen. Bei Patienten ohne überwiegende Negativsymptomatik ist der Zusatznutzen nicht belegt.
Schizophrenie ist eine Erkrankung, die durch Störungen verschiedener psychischer Bereiche wie Wahrnehmung, Denken, Ich-Funktionen, Affektivität, Antrieb und Psychomotorik gekennzeichnet ist. Dabei können akute psychotische Zustände episodisch auftreten, Beeinträchtigungen mit persistierenden Symptomen können auch chronifizieren. Es wird zwischen positiven (z. B. Wahn, Halluzinationen) und negativen Symptomen (z. B. Affektverflachung, Alogie, Anhedonie, Asozialität, Avolition) unterschieden, die aber auch gleichzeitig auftreten können.
Klinisch zu unterscheiden sind die Behandlung der Akutphase bei Erstmanifestation bzw. Rückfall und die Langzeitbehandlung zur Rezidivprophylaxe (1).
Cariprazin (Reagila®) ist zur Behandlung von Schizophrenie bei Erwachsenen zugelassen. Der Wirkmechanismus von Cariprazin ist nicht vollständig aufgeklärt. Es wird angenommen, dass die therapeutische Wirkung durch eine Kombination aus einem Antagonismus an Serotonin- (5-HT2B und 5-HT2A) und Histamin-H1-Rezeptoren sowie einem Partialagonismus an Dopamin- (D3 > D2) und Serotonin-Rezeptoren (5-HT1A) vermittelt wird. Cariprazin weist keine nennenswerte Affinität zu den Serotonin-5-HT2C-Rezeptoren, α1-Adrenozeptoren und cholinergen Muskarinrezeptoren auf. Cariprazin und seine zwei pharmakologisch aktiven Metabolite haben eine sehr lange Eliminationshalbwertzeit, die etwa eine Woche beträgt (2).
Für die Bewertung des Zusatznutzens ergaben sich zwei Fragestellungen, die sich aus den unterschiedlichen Therapiezielen bei der Behandlung von Patienten mit Schizophrenie ableiten: die Behandlung der akuten Symptomatik (etwa nach Exazerbation oder Erstdiagnose) und die Langzeitbehandlung/Rückfallprophylaxe einer stabilen Erkrankung. Der G-BA legte für das gesamte Anwendungsgebiet von Cariprazin als zweckmäßige Vergleichstherapie (ZVT) fest: Amisulprid oder Aripiprazol oder Olanzapin oder Paliperidon oder Quetiapin oder Risperidon oder Ziprasidon unter Berücksichtigung der oralen Formulierung und der Depotpräparate.
Dossierbewertung des IQWiG
In der Akutbehandlung waren die vom pU eingereichten Studien RGH-MD-04 und RGH-MD-16 aus Sicht des IQWiG nicht geeignet zur Ableitung des Zusatznutzens, da die Möglichkeit einer flexiblen Dosisanpassung während der Studien nicht bestand. Eine patientenindividuelle Optimierung der untersuchten Therapien war daher nicht möglich, das starre Dosierungsregime entspricht aus Sicht des IQWiG nicht der klinisch üblichen Vorgehensweise.
In der Langzeitbehandlung/Rückfallprophylaxe berücksichtigte das IQWiG die beiden Studien RGH-188-005 und A002-A7 im Vergleich zu Risperidon bei Patienten mit stabiler chronischer Schizophrenie und überwiegender Negativsymptomatik. Die Studie A002-A7 konnte nicht zur Bewertung des Zusatznutzens herangezogen werden, da die Rate der vorzeitigen Therapieabbrüche sehr hoch und auch bedeutsam unterschiedlich zwischen den Behandlungsarmen war und aus den Studienunterlagen sich kein nachvollziehbarer Grund dafür ergab. Aufgrund der signifikanten Verbesserung unter Cariprazin im Endpunkt psychosoziales Funktionsniveau (PSP-Gesamtscore) in der RGH-188-005-Studie ergab sich für die Patienten mit überwiegender Negativsymptomatik ein Anhaltspunkt für einen nicht quantifizierbaren Zusatznutzen von Cariprazin im Vergleich zur ZVT (3).
Im Rahmen der mündlichen Anhörung forderte der G-BA den pU auf, verwertbare Daten zum Endpunkt Akathisie aus der Studie RGH-188-005 nachzureichen. Die Bewertung dieser Daten führte aber nicht zu einer Änderung der Aussage des IQWiG zum Zusatznutzen von Cariprazin, da sich kein statistisch signifikanter Unterschied zwischen den Behandlungsgruppen zeigte (4).
Stellungnahme der AkdÄ
Die AkdÄ stimmte dem IQWiG zu, dass der Zusatznutzen in der Akutbehandlung nicht belegt ist, wies aber darauf hin, dass die vom IQWiG bemängelte fehlende Möglichkeit zur individuellen Dosisanpassung – wenn auch methodisch nachvollziehbar – in ihrer Ausschließlichkeit nicht gerechtfertigt ist. Für gut kontrollierte und zulassungsrelevante Studien zu einer definierten Fragestellung ist eine permanente Dosisanpassung über einen breiten Dosisbereich unter Beibehaltung der Verblindung praktisch nicht durchführbar. Eine beschränkte Anpassung, wie sie in der Studie RGH-188-005 vorgenommen wurde, ist aus Sicht der AkdÄ als angemessen zu bewerten. Bei Cariprazin ist zudem eine häufige und kurzfristige Dosisanpassung aufgrund der langen Eliminationshalbwertzeit unwirksam und unangebracht.
In der Studie zur Langzeitbehandlung/Rückfallprophylaxe bei Patienten mit überwiegender Negativsymptomatik erreichten 69,2 % der Patienten im Cariprazin-Arm und 58,1 % der Patienten im Risperidon-Arm eine mindestens 20-prozentige Verbesserung der Negativsymptomatik, gemessen anhand des PANSS-FNS (OR 2,08; 95 % CI 1,30–3,31; p = 0,0022). Der Effekt ist aus Sicht der AkdÄ als spezifisch und nicht verzerrt anzusehen, da Verzerrungen durch psychotische, depressive und extrapyramidalmotorische Symptome ausgeschlossen wurden. Dieser statistisch signifikante Unterschied ist daher aus Sicht der AkdÄ – im Gegensatz zur Einschätzung des IQWiG – patientenrelevant.
Die AkdÄ wies zudem darauf hin, dass die Frage, ob ein beobachteter Effekt klinisch relevant ist, keine rein statistische Frage ist, sondern dass sie auch aus dem klinischen Kontext heraus zu bewerten ist. Der beobachtete statistisch signifikante Unterschied entspricht mit einer Effektgröße von 0,31 einem kleinen bis mittelgroßen Effekt (5). Es muss aber auch berücksichtigt werden, dass primäre Negativsymptome und kognitive Störungen das größte therapeutische Problem bei der Behandlung der Schizophrenie darstellen und die soziale, berufliche und familiäre Prognose der Patienten und damit ihre Lebensqualität bestimmen. Eine therapeutische Wirkung auf Negativsymptome ist dementsprechend von hoher Patientenrelevanz. Die Effektgröße für die psychosoziale Funktion ist mit 0,48 (p < 0,0002; PSP) mittelgroß (5). Es sprachen 11 % mehr Patienten auf Cariprazin als auf Risperidon an, entsprechend einer Number needed to treat (NNT) von 9 (6). Zur Rückfallhäufigkeit und gesundheitsbezogenen Lebensqualität lagen keine validen Daten vor.
Bezüglich der Schadensendpunkte wie unerwünschte Ereignisse (UE), schwerwiegende UE, schwere UE vom Grad ≥ 3, Therapieabbrüche aufgrund UE sowie UE von besonderem Interesse (häufige UE, schwerwiegende SUE und Klasseneffekte) bestanden keine signifikanten Unterschiede. Akathisie trat unter Cariprazin nummerisch häufiger auf (8,3 % vs. 5,2 %), dagegen bestehen Anhaltspunkte für ein günstigeres Schadensprofil bezüglich QT-Zeit-Verlängerung, metabolischen Parametern und Prolaktinerhöhung. Insgesamt ist aus Sicht der AkdÄ ein höherer Schaden für Cariprazin nicht belegt. In der Gesamtschau bestand daher ein mindestens geringer Zusatznutzen für die Patienten mit überwiegender Negativsymptomatik. Die qualitative Ergebnissicherheit war aus Sicht der AkdÄ mäßig, da lediglich eine Studie zur Negativsymptomatik mit einem kleinen Effekt vorlag, sodass ein Anhaltspunkt für einen Zusatznutzen vorlag (7).
Beschluss des G-BA
Der G-BA beschloss, dass in der Langzeitbehandlung/Rückfallprophylaxe für Patienten mit überwiegender Negativsymptomatik aufgrund des statistisch signifikanten Effekts von Cariprazin im Endpunkt psychosoziales Funktionsniveau ein Hinweis für einen geringen Zusatznutzen besteht. Zusätzlich wurden die Ergebnisse bezüglich des Gesamteindrucks der Krankheitsschwere (anhand der Clinical global Impression Skala) unterstützend einbezogen. Die klinische Relevanz der Effekte im Endpunkt Negativsymptomatik (PANSS-Negativskala und PANSS-FNS) war aus Sicht des G-BA fraglich. In der Gesamtbetrachtung wurden die Effekte von Cariprazin als bisher gegenüber der ZVT nicht erreichte moderate und nicht nur geringfügige Verbesserung des therapierelevanten Nutzens bewertet. Aufgrund des randomisierten und verblindeten Designs der Studie RGH-188-005 wurde das Verzerrungspotenzial der Ergebnisse als gering und die Aussagesicherheit daher als Hinweis eingestuft.
In der Akutbehandlung sowie in der Langzeitbehandlung von Patienten ohne überwiegende Negativsymptomatik beschloss der G-BA, dass der Zusatznutzen nicht belegt ist (8).
Literatur
- Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften e. V. (AWMF), Deutsche Gesellschaft für Psychiatrie PuND: S3-Praxisleitlinien in Psychiatrie und Psychotherapie. Band 1 – Behandlungsleitlinie Schizophrenie. November 2005: www.awmf.org/uploads/tx_szleitlinien/038-009k_S3_Schizophrenie_01.pdf (letzter Zugriff: 25. September 2018). Kurzfassung, gültig bis November 2010.
- Recordati Pharma GmbH: Fachinformation "Reagila® Hartkapseln". Stand: Dezember 2017.
- IQWiG-Berichte – Nr. 646: Cariprazin (Schizophrenie) – Nutzenbewertung gemäß § 35a SGB V: www.iqwig.de/de/projekte-ergebnisse/projekte/arzneimittelbewertung/2018/a18-25-cariprazin-schizophrenie-nutzenbewertung-gemaess-35a-sgb-v.9568.html. Letzter Zugriff: 10. Oktober 2018.
- IQWiG-Berichte – Nr. 662. Cariprazin (Schizophrenie) – Addendum zum Auftrag A18-50: www.iqwig.de/de/projekte-ergebnisse/projekte/arzneimittelbewertung/2018/a18-50-cariprazin-schizophrenie-addendum-zum-auftrag-a18-25.10286.html. Letzter Zugriff: 10. Oktober 2018.
- Marder SR, Daniel DG, Alphs L et al.: Methodological issues in negative symptom trials. Schizophr Bull 2011; 37: 250-254.
- Leucht S, Davis JM: Schizophrenia, primary negative symptoms, and soft outcomes in psychiatry. Lancet 2017; 389: 1077-1078.
- Arzneimittelkommission der deutschen Ärzteschaft. Stellungnahme zu Cariprazin (Schizophrenie), Nr. 646, Auftrag A18-25, Version 1.0, Stand: 12. Juli 2018: www.akdae.de/Stellungnahmen/AMNOG/A-Z/Cariprazin/Cariprazin-EB.pdf. Letzter Zugriff: 10. Oktober 2018.
- Gemeinsamer Bundesausschuss: Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII – Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach § 35a SGB V – Cariprazin. 4. Oktober 2018. www.g-ba.de/downloads/40-268-5293/2018-10-04_AM-RL-XII_Cariprazin_D-354_TrG.pdf. Letzter Zugriff: 10. Oktober 2018.
„Neue Arzneimittel“ ist eine Information der Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ) zu neu zugelassenen Arzneimitteln oder zu neu zugelassenen Indikationen. Ziel ist es, den Ärzten zeitnah Informationen zu diesen Arzneimitteln zur Verfügung zu stellen, zunächst bei Markteinführung sowie nach der frühen Nutzenbewertung durch den Gemeinsamen Bundesausschuss (G-BA) (§ 35a Absatz 1 SGB V). „Neue Arzneimittel“ bei Markteinführung enthält Informationen basierend auf dem Europäischen Öffentlichen Bewertungsbericht (EPAR) der Europäischen Arzneimittel-Agentur (EMA) sowie weiteren bei Markteinführung vorliegenden Daten aus klinischen Studien. Nach Abschluss der frühen Nutzenbewertung wird der Zusatznutzen des neuen Arzneimittels und seine therapeutische Bedeutung auf der Basis der Dossierbewertung des IQWiG, der Stellungnahme der AkdÄ und des Beschlusses des G-BA im Rahmen der frühen Nutzenbewertung dargestellt („Update – Neue Arzneimittel“).
vorab online
Dieser Artikel wurde am 13. November 2018 vorab online veröffentlicht.
