Chronische Hepatitis C: Umwälzungen in der Therapie durch direkt antiviral wirkende Substanzen
Zusammenfassung
Etwa 300.000 Menschen sind in Deutschland von einer chronischen Hepatitis C betroffen, aus der sich soziale Deprivation, Fatigue-Syndrom, extrahepatische Manifestation, Leberzirrhose und hepatozelluläres Karzinom entwickeln. Daher wird bei jedem Betroffenen grundsätzlich die Indikation zur Therapie gesehen. Die bisherigen interferonbasierten Behandlungsprotokolle waren aufgrund der Abhängigkeit der Wirksamkeit von Genotyp, Ausprägung des Leberumbaus, Begleiterkrankungen und den zahlreichen Nebenwirkungen der Therapie nur in einem kleineren Anteil der Patienten anwendbar. Im Gegensatz dazu bietet die aktuelle, interferonfreie Kombinationsbehandlung mit direkt antiviral wirkenden Substanzen (DAA) eine Heilungswahrscheinlichkeit von deutlich über 90 %. Rückfälle sind selten. Die Therapie wird gut vertragen. Trotzdem muss festgestellt werden, dass unsere Kenntnisse bezüglich unerwünschter Arzneimittelwirkungen aufgrund der Zahl der bisher Behandelten noch eingeschränkt sind. Die Auswahl der richtigen Kombination aus DAA und die Kosten erfordern die Therapieführung durch einen spezialisierten Arzt. Eine gesamtgesellschaftliche Betrachtung der Kosten-Nutzen-Analyse dieser sehr teuren Therapie ist nicht Gegenstand dieser Publikation.
Abstract
About 300,000 people in Germany suffer from chronic hepatitis C form. Patients are at risk for social deprivation, fatigue syndrome, extrahepatic manifestations, cirrhosis and hepatocellular carcinoma. Hence, the indication for treatment is seen with every affected person. The effectiveness of the former interferon-based protocols depends of the effectiveness on the genotype, grade of histologic liver changes, accompanying illnesses and the numerous side effects of the therapy. So only a smaller portion of the patients could be treated with success. By contrast, the actual interferon-free combination treatment with direct acting antiviral substances (DAA) offers healing rates clearly above 90 %. Relapses are rare. The therapy is well tolerated. Nevertheless, our knowledge regarding side effects is still limited due to the limited number of treated patients. For the choice of an optimal combination of DAAs and because of the costs of therapy, guidance of treatment should be done by a specified doctor. The whole social consideration of the cost-benefit analysis of this very expensive therapy is not an object of this publication.
Epidemiologie und Ätiologie
Ca. 3 % der Weltbevölkerung sind mit dem Hepatitis-C-Virus (HCV) infiziert. Schätzungen für Deutschland belaufen sich auf ca. 300.000 chronisch HCV-Infizierte. In den Industrieländern der westlichen Hemisphäre ist das HCV eine wesentliche Ursache einer chronischen Hepatitis, einer Leberzirrhose und des hepatozellulären Karzinoms. Diese Folgeerkrankungen der chronischen HCV-Infektion, deren Häufigkeitspeak erst in den nächsten 10–15 Jahren erwartet wird, sind eine der Hauptindikationen für eine Lebertransplantation.
Das Hepatitis-C-Virus ist ein RNA-Flavivirus. Es werden sechs Genotypen und 80 Subtypen unterschieden, deren Häufigkeit regional deutlich variiert. In Deutschland findet man überwiegend den Genotyp 1 mit knapp 80 %. Die verbleibenden 20 % verteilen sich überwiegend auf Genotyp 2 und 3, seltener Genotyp 4. Die Genotypen 5 und 6 sind mit unter einem Prozent in Deutschland zahlenmäßig nicht von Bedeutung. Die Übertragung des Virus erfolgt parenteral oder sexuell. Risikofaktoren sind (intravenöser) Drogenabusus und hygienische medizinische Prozeduren (zum Beispiel bei Piercing oder Tattoos). Der sexuelle Transmissionsweg ist im Wesentlichen nur bei Männern, die Sex mit Männern haben, quantitativ von Bedeutung. Bei einem relevanten Anteil der Erkrankten lässt sich kein typischer Übertragungsweg eruieren (10–50 %).
Klinik und Verlauf
Leistungsminderung und körperliche Abgeschlagenheit (Fatigue) sind die häufigsten Symptome bei der chronischen Hepatitis C; meist verläuft die Erkrankung jedoch über Jahre asymptomatisch. Aber auch bei asymptomatischem Verlauf und/oder normalen Transaminasen ist ein Fortschreiten der Erkrankung bis zur Zirrhose möglich. Die chronische Hepatitis-C-Infektion kann eine Reihe extrahepatischer Manifestationen zeigen (zum Beispiel vaskulitische Purpura, gemischte Kryoglobulinämie, membranoproliferative Glomerulonephritis, Gelenkbeschwerden).
Drei Viertel der akuten Hepatitis-C-Infektionen verlaufen asymptomatisch und werden daher selten diagnostiziert. 60–85 % aller Patienten mit einer akuten Infektion entwickeln eine chronische Hepatitis C. Etwa ein Drittel der chronischen Infektionen verläuft ohne histologische Leberveränderungen, ein Drittel zeigt einen langsam progredienten Verlauf mit einer Zirrhoseentwicklung nach ca. 30 Jahren und ein Drittel zeigt eine raschere Progredienz mit Ausbildung einer Zirrhose innerhalb von zehn Jahren. In dieser Gruppe finden sich insbesondere Patienten mit zusätzlichen hepatotoxischen Noxen wie Alkohol oder einer HBV-Koinfektion, signifikant gehäuft aber auch Personen jenseits des 40. Lebensjahres, Männer, immunsupprimierte Patienten, Patienten mit Adipositas bzw. Insulinresistenz und solche, die sich durch Blutprodukte infiziert haben. Bei den Personen mit HCV-induzierter Zirrhose erleben innerhalb von zehn Jahren ca. ein Drittel eine Dekompensation und pro Jahr entwickeln 1–5 % ein hepatozelluläres Karzinom.
Diagnose
Die Diagnose einer HCV-Infektion wird durch den Nachweis von Antikörpern mittels ELISA und von Virus-RNA mit PCR geführt. Die Bestimmung des Genotyps vor Therapiebeginn ist Standard. Dagegen ist die Quantifizierung der Viruslast durch die neuen Therapieoptionen vor Einleitung einer Behandlung nur noch in definierten Situationen notwendig. Eine Leberhistologie ist für die Diagnose und die Indikationsstellung zur Therapie nicht mehr erforderlich, hat aber Implikationen für die Medikamentenauswahl und die Therapiedauer, sofern histologisch eine Zirrhose bereits vorliegt. Durch eine Elastographie können die Patienten zur Biopsie selektioniert werden, bei denen mit fortgeschrittenen morphologischen Veränderungen zu rechnen ist.
Therapieindikation und Zielsetzung der Behandlung
Die chronische Hepatitis C ist aufgrund der oben beschriebenen assoziierten Morbidität und Mortalität eine grundsätzlich behandlungsbedürftige Erkrankung. In jedem Einzelfall sollte unter Berücksichtigung von Nutzen, Risiken und Kontraindikationen die Indikation für eine antivirale Therapie geprüft und diese dann auch durchgeführt werden. Die Vermeidung der Entwicklung einer Zirrhose und eines hepatozellulären Karzinoms und die Senkung damit verbundener Mortalität sind die eigentlichen Endpunkte der Behandlung (wobei eine mögliche soziale Deprivation infolge des chronischen Virusinfekts für die Betroffenen ebenfalls sehr relevant ist). Aufgrund der teilweise Jahrzehnte messenden Latenz sind diese Parameter aber im klinischen Alltag nicht als Messpunkte für einen Therapieerfolg geeignet. Surrogatparameter für eine erfolgreiche Therapie ist eine negative Virus-PCR zwölf Wochen nach Therapieende (Sustained Viral Response nach 12 Wochen = SVR12). Langzeitstudien bestätigen, dass diese SVR12 mit signifikant verminderter Progression einer Fibrose und Mortalität verknüpft ist.
Interferonbasierte Therapie in der Vergangenheit
Zu Beginn des neuen Jahrtausends wurde mit der Einführung einer interferonbasierten Therapie (in Kombination mit Ribavirin) erstmals eine Heilung der chronischen Hepatitis C möglich. Etwa die Hälfte der Patienten mit chronischer Hepatitis C mit Genotyp 1 konnten durch diese Kombination eine Heilung erwarten. Über 95 % der Patienten mussten jedoch mit beeinträchtigenden und relevanten Nebenwirkungen der teilweise über ein Jahr geführten Therapie rechnen. Diese reichten von grippalen Symptomen, autoimmunen Phänomenen mit z. B. Entwicklung einer Hypothyreose bis zur Entwicklung einer Depression. Die Abbruchrate einer interferonbasierten Therapie liegt bei ca. 15 %. Ribavirin erfordert eine konsequente Kontrazeption bis sechs Monate nach Therapie und verursacht bei jedem dritten Behandelten eine Anämie. 2012 wurden mit Telaprevir und Boceprevir die ersten Proteinaseinhibitoren in die Behandlung eingeführt. Je nach Genotyp konnten hierdurch bis 75 % der Behandelten geheilt werden, allerdings mit einem sehr strikt einzuhaltenden und immer noch durch erhebliche Nebenwirkungen beeinträchtigten Behandlungsregime.
Aktuelle, interferonfreie Therapie
Die Einführung einer interferonfreien Behandlung der chronischen Hepatitis C mit direkt wirkenden antiviralen Arzneimitteln (directly acting antivirals, DAA) hat die Therapie der chronischen Hepatitis C seit Mitte 2015 grundlegend verändert: Interferonfreie Behandlungsregime haben deutlich weniger Nebenwirkungen und erreichen bei deutlich mehr Patienten eine SVR – und dies bei kürzerer Behandlungsdauer. Zudem können viele Patienten, bei denen Kontraindikationen gegen die Behandlung mit Interferon früher eine Behandlung unmöglich gemacht hätten, heute interferonfrei und erfolgreich mit DAA behandelt werden.
Die mit Nebenwirkungen belasteten und weniger effektiven interferonbasierten Behandlungsregime werden in den aktuellen Leitlinien nicht mehr empfohlen, sind obsolet und werden nicht mehr eingesetzt.
Die neuen DAA werden anhand ihres Angriffspunktes am Virus unterteilt in Proteinaseinhibitoren (zum Beispiel Simeprevir, Paritaprevir/Ritonavir), NS5A-Inhibitoren (z. B. Daclatasvir, Ombitasvir, Velpatasvir), nichtnukleosidische Polymeraseinhibitoren (NNPI; z. B. Dasabuvir) und nukleosidische Polymerase(BS5B)-Inhibitoren (z. B. Sofosbuvir) (siehe Tabelle 1).
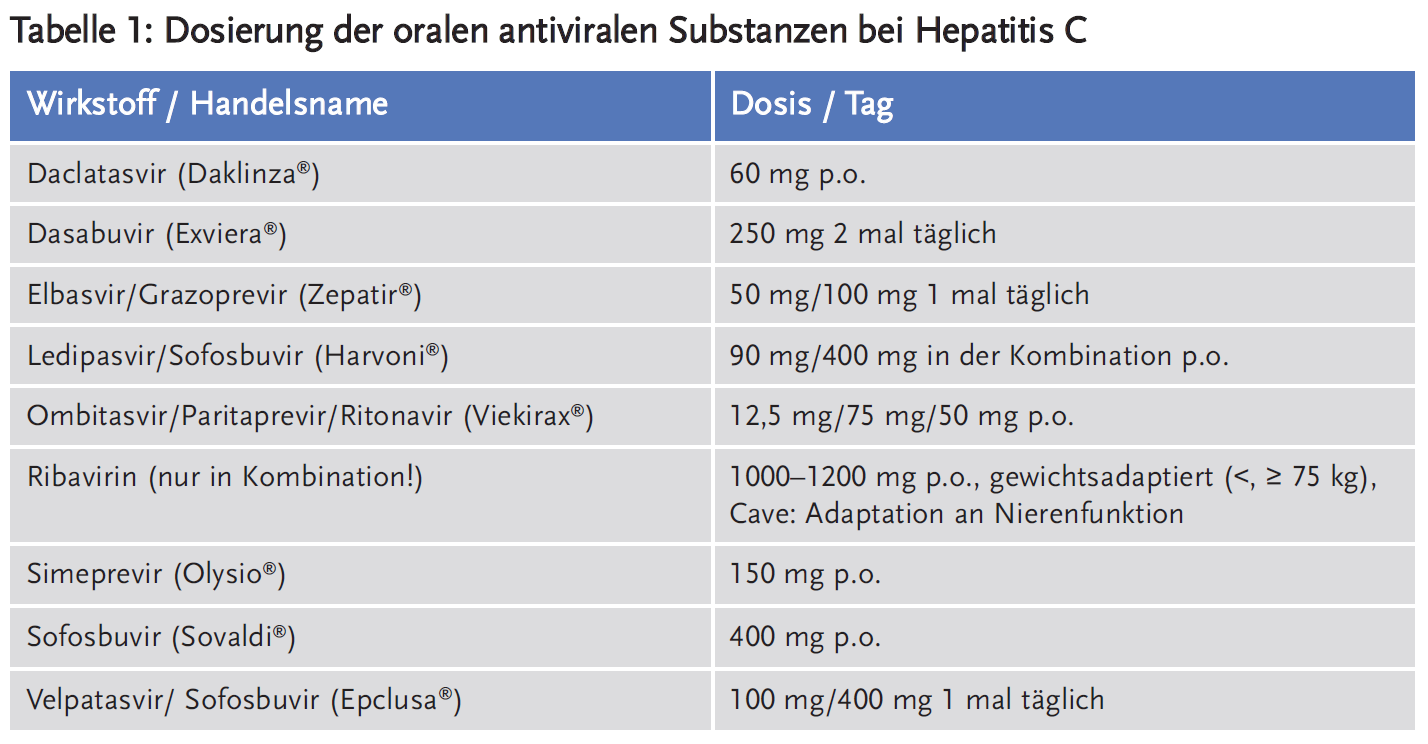
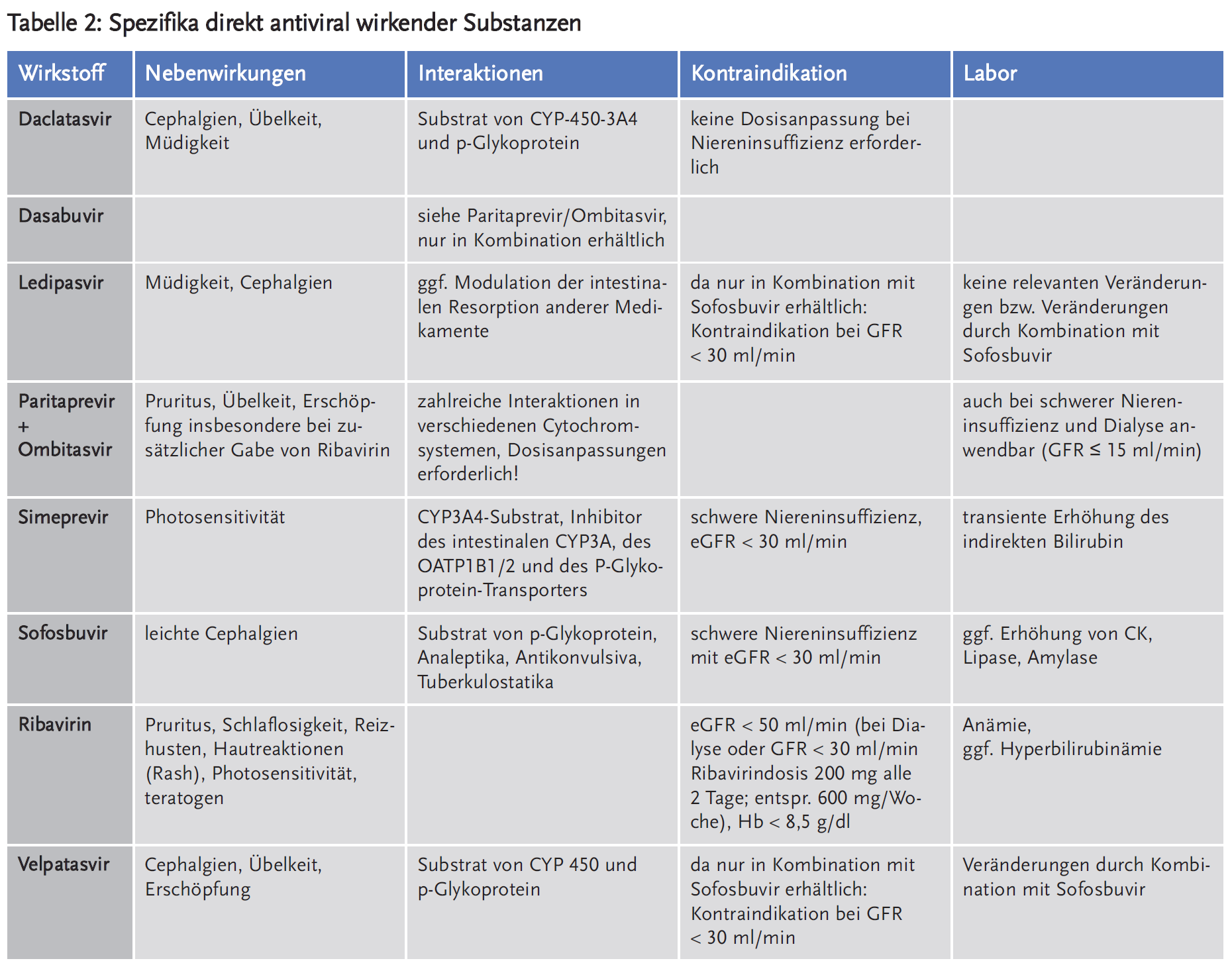
Arzneimittelwechselwirkungen sind bei allen DAA zu beachten, dies gilt insbesondere für die Proteaseinhibitoren (siehe Tabelle 2). Neben den Fachinformationen finden sich aktuelle Hinweise hierzu unter www.hep-druginteractions.org (Universitätsklinik Liverpool). Keine der Substanzen hat eine Zulassung in der Schwangerschaft, sodass eine strenge Kontrazeption indiziert ist (wie bereits erwähnt, bei Ribavirin sechs Monate über das Therapieende hinaus). Es gibt Einzelfallberichte über eine Reaktivierung einer chronischen Hepatitis B unter der Therapie der Hepatitis C mit DAA sowie Hinweise, ebenfalls aus Einzelfällen, dass es nach erfolgreicher Hepatitis-C-Therapie durch den Wegfall der Stimulation des Immunsystems infolge des chronischen Infektes zu einem beschleunigten Progress bereits manifester (mikroskopischer) hepatozellulärer Karzinome kommen kann.
Die Auswahl und Dauer der Therapie mit DAA ohne oder in Kombination mit Ribavirin wird im Wesentlichen durch den Genotyp des HCV bestimmt, wobei bei dem HCV-Genotyp 1 auch der Subtyp (GT1a und GT1b) einen Einfluss auf die Erfolgswahrscheinlichkeit und Auswahl der Therapie hat. Für einzelne Therapieschemata und Patientengruppen ist zudem das Vorliegen und das Child-Pugh-Stadium einer Leberzirrhose zu beachten, die Vorbehandlung mit interferonbasierter oder interferonfreier DAA-Therapie, die Ausgangsviruslast (als Determinante der empfohlenen Therapiedauer) und die Möglichkeit einer DAA-Resistenz des HCV. Auch das Vorliegen einer Niereninsuffizienz ist bei der Therapieauswahl zu berücksichtigen wie auch das Risiko von Medikamenteninteraktionen zwischen DAA und weiteren bereits verordneten Arzneimitteln.
Die Therapie der chronischen Hepatitis C (CHC) ist damit wesentlich erfolgreicher und verträglicher geworden, die Entscheidung über das für den jeweiligen Patienten bestmögliche Therapieregime ist aber auch deutlich komplexer.
Behandlungsoptionen der CHC bei Genotyp 1
Der Genotyp 1 ist der in Deutschland am häufigsten auftretende Genotyp des HCV. Für seine Behandlung stehen zugelassene DAA-Kombinationsschemata zur Verfügung. Bei einigen Therapieschemata ist der Subtyp des HCV (GT1a oder GT1b) und für bestimmte Patientengruppen das Vorbestehen einer resistenzassoziierten Virusvariante (RAV) zu berücksichtigen.
Sofosbuvir + Velpatasvir (SVR12: 98 %)
Die Behandlung erfolgt über zwölf Wochen, auch bei Zustand nach Lebertransplantation. Bei dekompensierter Leberzirrhose ab Stadium Child B wird zusätzlich mit Ribavirin therapiert.
Simeprevir + Sofosbuvir (SVR12: 79–97 %)
Die Behandlung erfolgt über zwölf Wochen (Optimist-1- und -2-Studie). Die Therapieergebnisse sind bei Patienten mit Zirrhose schlechter (SVR12: 79–88 %) als bei Patienten ohne Zirrhose. Bei GT1a ist das Vorliegen von RAV zu berücksichtigen: Bei Patienten mit Q80K-Mutation wird eine SVR nur bei 74 % der Patienten erreicht.
Sofosbuvir + Ledipasvir (SVR12: 97–99 %)
Behandelt wird über zwölf Wochen bei Patienten ohne oder mit kompensierter Zirrhose, bei dekompensierter Zirrhose in Kombination mit Ribavirin. Der Subtyp des HCV hat keinen Einfluss auf die SVR-Wahrscheinlichkeit und das Therapieregime.
Eine Kombination mit Ribavirin wird auch für therapieerfahrene Patienten mit kompensierter Zirrhose empfohlen (SVR12: 96 %), da die SVR12 ansonsten nur 90 % beträgt. Alternativ kann eine 24-wöchige Sofosbuvir + Ledipasvir-Therapie bei vorbehandelten Patienten mit Zirrhose erfolgen (SVR12: 98–100 %).
Eine Therapieverkürzung auf acht Wochen ist bei weiblichem Geschlecht und bei Patienten ohne Zirrhose mit einer Ausgangsviruslast unter 6 Millionen IU/ml möglich. Bei IL28B-CC-Genotyp ist in der Kombination mit Ribavirin eine Therapieverkürzung auf acht Wochen möglich.
Paritaprevir/Ritonavir + Ombitasvir + Dasabuvir +/- Ribavirin (SVR12: 95–97 %)
Das Behandlungsregime ist vom Subtyp des HCV abhängig: Beim GT1b erfolgt die Behandlung ohne, beim GT1a immer in Kombination mit Ribavirin. Beim GT1b wird mit zwölfwöchiger Therapie unabhängig vom Vorliegen einer kompensierten Zirrhose eine SVR12 von 100 % beschrieben. Beim GT1a werden in Kombination mit Ribavirin SVR12-Raten von 96–99 % beschrieben. Eine Therapieverlängerung auf 24 Wochen bei negativen Prädiktoren für den Therapieerfolg wird empfohlen. Eine dekompensierte Leberzirrhose stellt eine Kontraindikation dar.
Daclatasvir + Sofosbuvir (SVR12: 94–98 %)
Patienten ohne Zirrhose werden über zwölf Wochen therapiert. Nach Lebertransplantation und bei Leberzirrhose erfolgt eine Kombination mit Ribavirin, in Abhängigkeit vom Zirrhosestadium über 12 bzw. 24 Wochen (bei Leberzirrhose im Stadium Child A/B ist auch eine Therapie ohne Ribavirin über 24 Wochen möglich).
Elbasvir + Grazoprevir (SVR12: 92–100 %)
Die Therapie erfolgt über zwölf Wochen. Schlechtere SVR12-Raten werden für Patienten mit GT1a und RAV beobachtet. Bei diesen Patienten ist eine Kombination mit Ribavirin möglich.
Behandlungsoptionen der CHC bei Genotyp 2
Sofosbuvir + Velpatasvir (SVR12: 99–100 %)
Die Behandlung erfolgt über zwölf Wochen, auch bei Zustand nach Lebertransplantation. Bei dekompensierter Leberzirrhose ab Stadium Child B wird zusätzlich mit Ribavirin therapiert.
Sofosbuvir + Ribavirin (SVR12: 86–97 %)
Behandelt werden Patienten ohne Zirrhose, die Behandlung erfolgt über zwölf Wochen.
Daclatasvir + Sofosbuvir (SVR12: 96–100 %)
Kann derzeit aufgrund der geringen Datenlage nicht als primäre Behandlungsoption empfohlen werden.
Behandlungsoptionen der CHC bei Genotyp 3
Der GT3 ist der zweithäufigste HCV-Genotyp in Deutschland und deutlich schwieriger zu behandeln als der GT1. Die Behandlung mit Sofosbuvir + Ribavirin wird gemäß AASLD(American Association for the Study of Liver Diseases)- und EASL(European Association for the Study of the Liver)-Leitlinien nicht mehr empfohlen.
Sofosbuvir + Velpatasvir (SVR12: 88–97 %)
Die Behandlung erfolgt über zwölf Wochen, auch bei Zustand nach Lebertransplantation. Bei dekompensierter Leberzirrhose ab Stadium Child B wird zusätzlich mit Ribavirin therapiert. Vorbehandelte Patienten ohne Zirrhose und alle Patienten mit kompensierter Zirrhose bei Nachweis (oder Unmöglichkeit des Ausschlusses) der resistenzassoziierten Substitution (RAS) NS5A RAS Y93H sollten zusätzlich mit Ribavirin behandelt werden. In der ASTRAL-3-Studie erreichten GT3-Patienten ohne/mit Y93H resistenzassoziierter Variante RAV ein SVR12 von 97 % bzw. 88 %. 16 % der eingeschlossenen Patienten wiesen eine Y93H RAV auf.
Daclatasvir + Sofosbuvir (SVR12: 63–96 %)
Patienten ohne Zirrhose werden für zwölf Wochen, Patienten mit Zirrhose für 24 Wochen behandelt. Das Vorliegen einer NS5A-Y93H-Mutation des HCV ist prognostisch bezüglich des Erreichens einer SVR ungünstig und wird in den ASSLD-Leitlinien (7/2016) neben Zustand nach Vorbehandlung als Kriterium für die Entscheidung zur Kombination mit Ribavirin benutzt. Bei Vorliegen einer NS5A-Y93H-Mutation des HCV werden mit zwölfwöchiger Daclatavir + Sofosbuvir-Therapie nur 63 % SVR12 erreicht (ALLY-3-Studie).
Behandlungsoptionen der CHC bei Genotyp 4
Der GT4 ist dem GT1 ähnlich, was sich in der Wirksamkeit der Therapieschemata widerspiegelt.
Sofosbuvir + Velpatasvir (SVR12: 100 %)
Die Behandlung erfolgt über zwölf Wochen, auch bei Zustand nach Lebertransplantation. Bei dekompensierter Leberzirrhose ab Stadium Child B wird zusätzlich mit Ribavirin therapiert.
Sofosbuvir + Ledipasvir (SVR12: ca. 95 %)
Behandelt wird über zwölf Wochen, auch bei Zirrhose, sofern diese kompensiert ist. Bei dekompensierter Zirrhose wird zusätzlich Ribavirin verordnet. Bei weiblichem Geschlecht oder bei Patienten ohne Zirrhose mit einer Ausgangsviruslast unter 6 Millionen IU/ml kann die Behandlung auf acht Wochen verkürzt werden.
Paritaprevir/Ritonavir + Ombitasvir + Ribavirin (SVR12: 100 %)
Behandlung über zwölf Wochen, bei kompensierter Zirrhose über 24 Wochen.
Daclatasvir + Sofosbuvir (SVR12: 94–98 %)
Patienten ohne Zirrhose werden über zwölf Wochen therapiert (bei Zustand nach Lebertransplantation in Kombination mit Ribavirin). Bei Leberzirrhose im Stadium Child A oder Child B wird entweder über zwölf Wochen in Kombination mit Ribavirin oder ohne Ribavirin über 24 Wochen therapiert. Die Kombination mit Ribavirin wird über 24 Wochen gegeben bei Child-Pugh-C-Zirrhose.
Elabasvir + Grazoprevir (SVR12 96 % ohne, 83 % mit Zirrhose)
Behandlung über zwölf Wochen, bei Patienten mit Zustand nach Vorbehandlung und Zirrhose in Kombination mit Ribavirin.
Behandlungsoptionen bei CHC bei Genotyp 5 und Genotyp 6
Sofosbuvir + Velpatasvir (SVR12: 97–100 %)
Die Behandlung erfolgt über zwölf Wochen, auch bei Zustand nach Lebertransplantation. Bei dekompensierter Leberzirrhose ab Stadium Child B wird zusätzlich mit Ribavirin therapiert.
Sofosbuvir + Ledipasvir (SVR12: 95 %)
Die Behandlung erfolgt unabhängig vom Vorliegen einer Zirrhose oder dem Vorbehandlungsstatus über zwölf Wochen, ist aber nur durch kleine Fallzahlen belegt.
Koinfektion mit HIV oder mit dem Hepatitis-B-Virus (HBV)
Eine Koinfektion mit HIV ändert die Behandlungsoptionen nicht. Bei einer Koinfektion mit HBV sind engmaschige Kontrollen notwendig, da eine Aktivierung der HBV-Infektion unter der Therapie mit DAA berichtet wurde.
Fazit für die Praxis
Die Behandlung einer chronischen Hepatitis C soll bei jedem Betroffenen erwogen werden. Die neuen Kombinationsbehandlungen mit direkt antiviral wirkenden Substanzen ermöglichen eine Heilung in über 90 % bei (nach heutigem Stand) guter Verträglichkeit. Indikationsstellung und Therapiebegleitung sollten durch den spezialisierten Arzt/Ärztin erfolgen, auch aufgrund der hohen Kosten.
Interessenkonflikte
U. Rosien erhielt Honorare für Fortbildungsveranstaltungen und Vorträge von Falk Foundation, AbbVie/Abbott und Olympus.
Ein Interessenkonflikt wird von D. Grandt verneint.
D. Frederking erhielt Reisekosten von AbbVie GmbH DGus und MSD Scharp GmbH sowie Honorare für eine Veranstaltung zum Thema Hepatitis.
Literatur
- Robert Koch-Institut (RKI): Aktuelle Statistik meldepflichtiger Infektionskrankheiten, 45. Woche 2009 (Datenstand: 25.11.2009). Epidemiol Bull 2009; Nr. 48: 500-502.
- Morgan RL, Baack B, Smith BD et al.: Eradication of hepatitis C virus infection and the development of hepatocellular carcinoma: a meta-analysis of observational studies. Ann Intern Med 2013; 158: 329-337.
- van der Meer AJ, Veldt BJ, Feld JJ et al.: Association between sustained virological response and all-cause mortality among patients with chronic hepatitis C and advanced hepatic fibrosis. JAMA 2012; 308: 2584-2593.
- World Health Organization (WHO): Guidelines for the screening, care and treatment of persons with chronic hepatitis C infection. Genf: WHO, April 2016.
- European Association for Study of Liver: EASL recommendations on treatment of hepatitis C 2015. J Hepatol 2015; 63: 199-236.
- Sarrazin C, Berg T, Buggisch P et al.: Aktuelle Empfehlung zur Therapie der chronischen Hepatitis C. Z Gastroenterol 2015; 53: 320-334.
- AASLD/IDSA HCV Guidance Panel: Hepatitis C guidance: AASLD-IDSA recommendations for testing, managing, and treating adults infected with hepatitis C virus. Hepatology 2015; 62: 932-954.
Hinweis
Dieser Artikel basiert auf einem Kapitel zur Hepatitis C aus dem Buch „Facharztwissen Gastroenterologie“ (Elsevier-Verlag 2017) und der Stellungnahme der AkdÄ zur Nutzenbewertung (nach AMNOG) von Sofosbuvir/Velpatasvir (November 2016).
