Acne vulgaris bei Jugendlichen und Erwachsenen
Rubrik: Therapie aktuell
Acne vulgaris
Etwa 85 % der Individuen im Alter von 12 bis 24 Jahren sind zeitweilig von der Akne vulgaris betroffen (1;2). Es wird unterschieden zwischen einer physiologischen und einer klinischen Akne. Physiologische Akne tritt bei ca. 40 % der Jugendlichen auf und geht nur mit wenigen Komedonen und entzündlichen Effloreszenzen einher. Sie wird in der Regel durch nicht verschreibungspflichtige Präparate behandelt und zeigt nur einen relativ kurzen Verlauf (3). Die klinische Akne, die die anderen 60 % ausmacht, bedarf hingegen der ärztlichen Beratung und Behandlung. Zur Pathologie, Verlauf, Diagnostik und Klinik wird auf die Referenzen (1-4) verwiesen. Eine Rolle bei der Entstehung spielen vor allem gesteigerte Seborrhö und follikuläre Hyperkeratose, daneben eine Dysbiose des Hautmikrobioms und seboglanduläre Entzündungsprozesse. Weiterhin können endogene Faktoren wie z. B. eine hormonelle Dysregulation und exogene Faktoren wie z. B. Ernährung, mechanische Irritation und kosmetische Externa aggravierend wirken und die Ausprägung des Krankheitsbildes beeinflussen (3).
Therapie
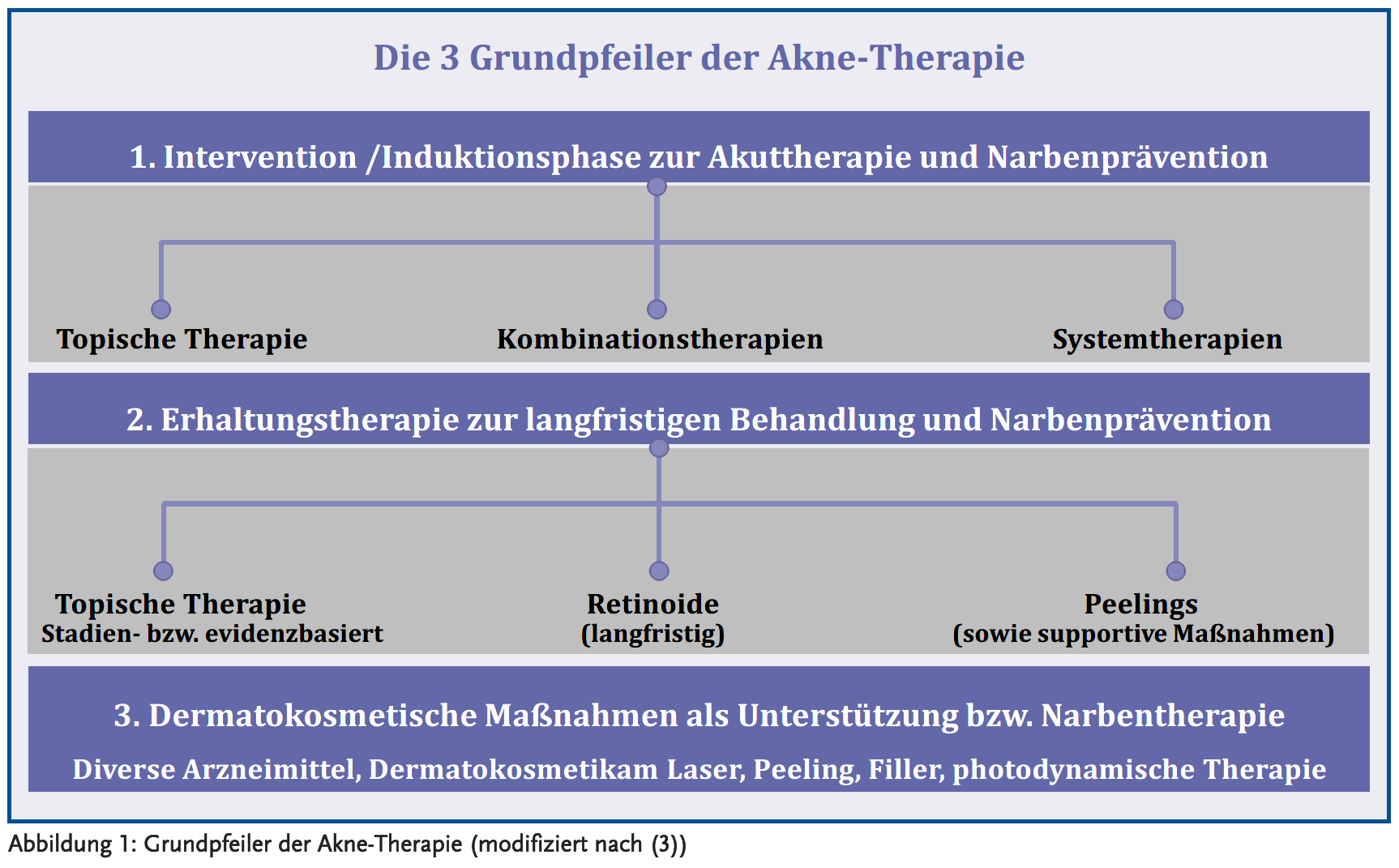
Bei der Therapie ist grundsätzlich zu unterscheiden: (a) die akute Interventions- und (b) die Erhaltungstherapie mit topischen und systemisch wirksamen Arzneimitteln bzw. ihre Kombinationen (siehe Abbildung 1).
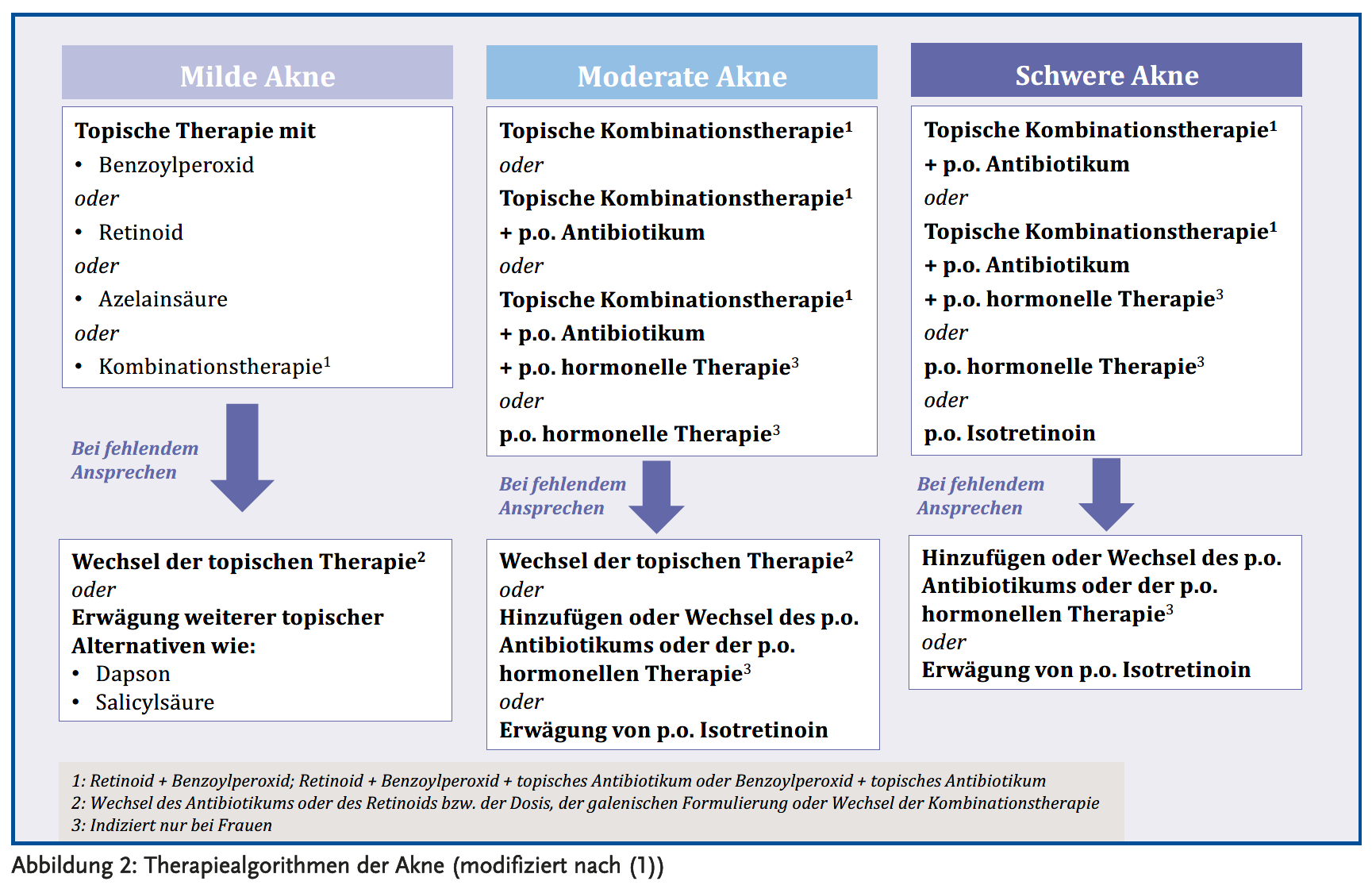
Die Intervention richtet sich nach der Art und der Schwere des Befundes. Als Kriterien angewendet werden: Schweregrad, Anzahl und Art der Läsionen, Ort des Befalls, Vernarbung, familiäre Belastung, Geschwindigkeit des Auftretens, psychischer und psychosozialer Einfluss. Hierbei wird zumeist eine Auswahl getroffen. Bei einer moderaten Akne unter oralem Tetrazyklin (z. B. Doxycyclin) plus topischem Benzoylperoxid tritt in etwa 50 % der Fälle Besserung nach drei Monaten ein. Bei milderen Verläufen mit topischer Therapie ist auch ein schnelleres Ansprechen möglich, schwere klinische Verläufe brauchen entsprechend länger (3). Mögliche, nicht validierte Therapiealgorithmen sind in Abbildung 2 modifiziert nach (1) dargestellt.
Topische Therapien
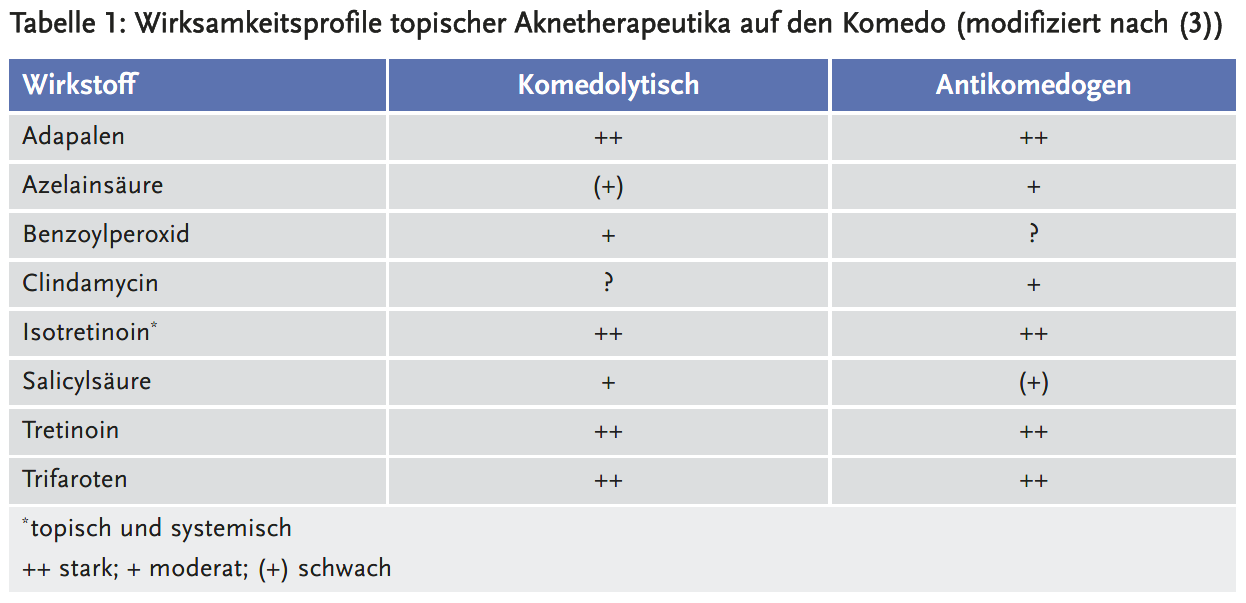
Die meistgenutzten Externa in der Aknetherapie sind Benzoylperoxid (BPO), Retinoide (All-trans-Retinsäure, 13-cis-Retinsäure, Adapalen, Tazaroten (derzeit in Deutschland nicht verfügbar), Trifaroten), salicylsäurehaltige Präparate, Antibiotika (Clindamycin, Erythromycin), Azelainsäure (antikomedogen als auch antiinflammatorisch wirksam; auch in Kombination mit oralem Minocyclin oder oralem Isotretinoin) und topische Kombinationspräparate, die insbesondere bei der Acne papulopustulosa eingesetzt werden, zum Beispiel mit der Kombination zweier Wirkstoffe (z. B. Clindamycin/BPO; Adapalen/BPO) (3). In Tabelle 1 sind die Wirksamkeitsprofile der topischen Aknetherapeutika dargestellt.
Systemische Therapien
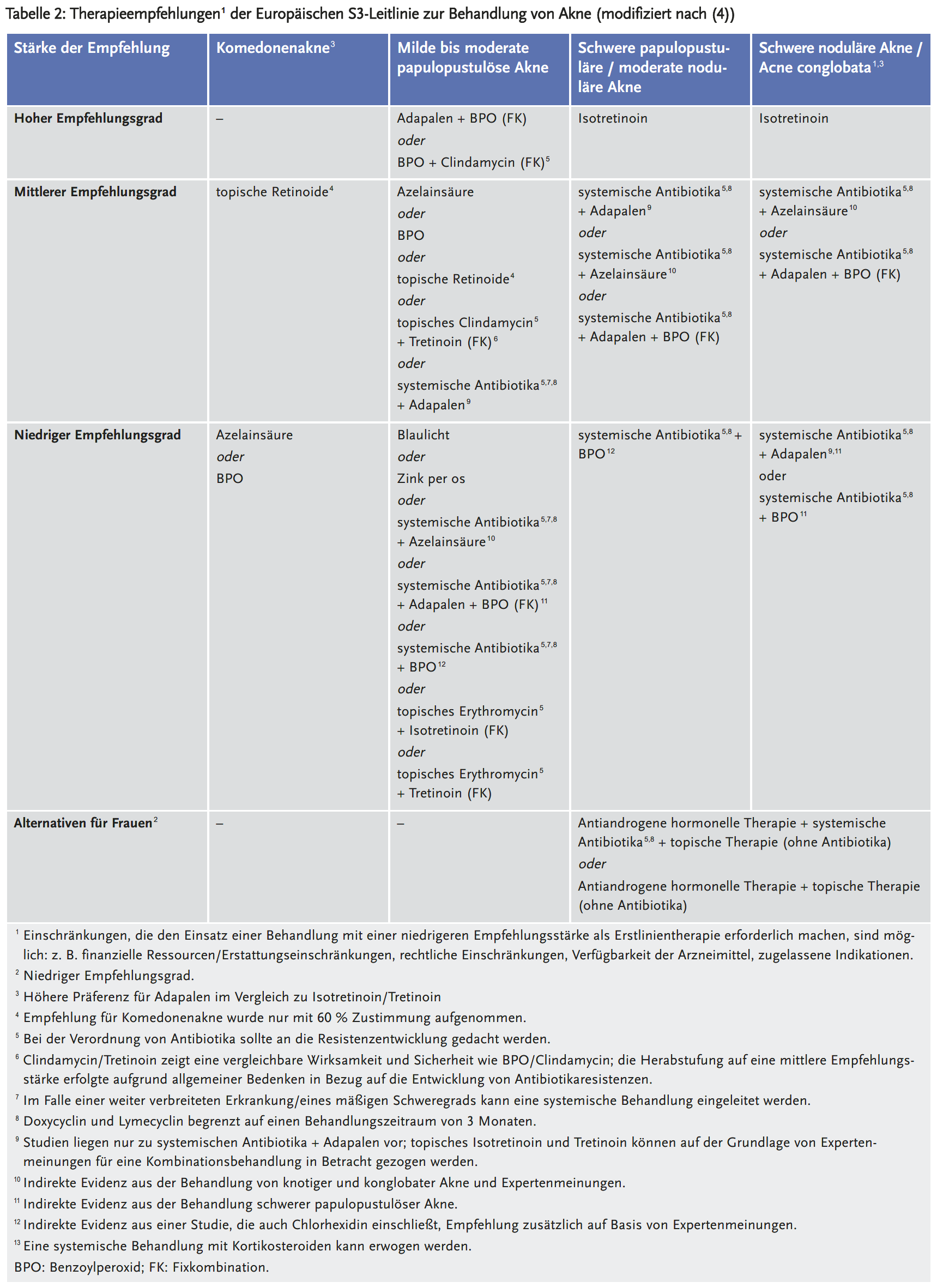
Systemische Therapien sind indiziert bei unbefriedigendem Erfolg der topischen Therapien (siehe Abbildung 2). Es handelt sich dabei um Antibiotika, die neben der antibiotischen Wirkung auch entzündungshemmende Effekte aufweisen (sogenannter paraantibiotischer Effekt), und systemisch wirksame Retinoide (vor allem Isotretinoin). Wegen der Gefahr der Resistenzentwicklung sollte der Einsatz von Antibiotika die Dauer von zwölf Wochen nicht überschreiten. Wegen der teratogenen Wirkung der Retinoide unterliegt ihr Einsatz bei Frauen im gebärfähigen Alter einem strengen Überwachungsregime (siehe Kasten), wenn sich Arzt und Patientin auf ihren Einsatz verständigen. Hierbei ist auf einen ausreichenden, mindestens doppelt greifenden Verhütungsschutz zu achten sowie auf eine mindestens einmonatige Verhütung nach Absetzen (3). Vorgeschaltet sein sollte eine gut wirksame, antiandrogene Therapie mit hormonellen Kontrazeptiva, deren Wirkung allerdings erst mit Verzögerung eintritt (1;5), die allerdings nur eingesetzt werden sollten, wenn gleichzeitig die Kontrazeption gewünscht wird, da deren Einsatz die Gefahr von Herz/Kreislauf-Komplikationen mit sich bringt. Bei alleiniger Therapie der Akne würde sich das Nutzen-Risiko-Verhältnis verschieben (Risiko: vor allem kardiovaskuläre Ereignisse wie venöse Thromboembolien (2)). In Tabelle 2 sind die Empfehlungen der Europäischen S3-Leitlinie zur Behandlung von Akne zusammengefasst (4).
Die US-amerikanischen Empfehlungen „The American Academy of Dermatology’s 2016 guidelines for the management of acne vulgaris“ wurden 2024 überarbeitet und mit einem systematischen Review ergänzt, aus dem 18 evidenzbasierte Empfehlungen und fünf Gute-Praxis-Aussagen (Good Practice Statements) abgeleitet wurden (2). Starke Empfehlungen werden dabei ausgesprochen für topisches Benzoylperoxid, Retinoide und/oder Antibiotika und ihre Fixkombinationen sowie für systemische Gabe von Doxycyclin (p.o.). Systemisches Isotretinoin (p.o.) wird empfohlen bei schwerer Akne, bei Akne, die psychosoziale Belastung oder Narbenbildung verursacht, oder bei Akne, bei der die Standardbehandlung mit oraler oder topischer Therapie versagt hat. Bedingte Empfehlungen werden ausgesprochen für die Anwendung von topischem Clascoteron, Salicylsäure, Azelainsäure, oralem Minocyclin, Sarecyclin, kombinierten oralen Kontrazeptiva und Spironolacton.
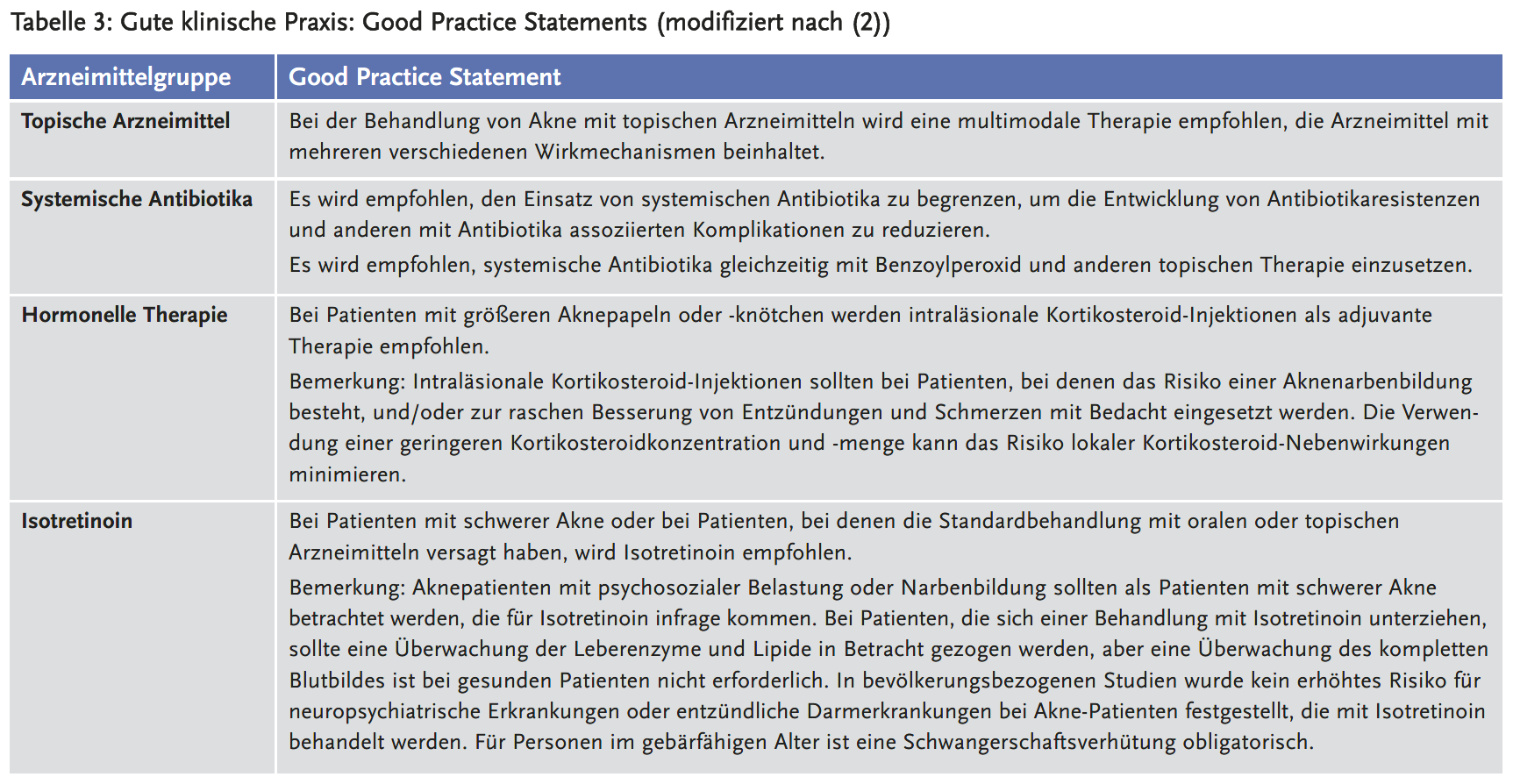
Als gute klinische Praxis gelten die Anwendung von topischen Therapien, die mehrere Wirkmechanismen kombinieren, die Begrenzung der Verwendung systemischer Antibiotika, die Kombination von systemischen Antibiotika mit Benzoylperoxid und anderen topischen Therapien und adjuvante intraläsionale Kortikosteroid-Injektionen (2) (siehe Tabelle 3).
Ausblick
Sarecyclin
Sarecyclin (Seysara™) ist ein einmal täglich oral einzunehmendes Arzneimittel der Tetracyclin-Klasse. Es wurde bereits 2018 in den USA für die Behandlung von entzündlichen Läsionen der nicht knotigen mittelschweren bis schweren Akne vulgaris bei Patienten im Alter von ≥ 9 Jahren zugelassen. Sarecyclin ist ein Ribosomenprotein-Inhibitor, der in vitro eine starke Wirksamkeit gegen P. acnes und andere grampositive Bakterien sowie entzündungshemmende Wirkungen gezeigt hat. Der genaue Wirkmechanismus von Sarecyclin bei der Behandlung von Akne vulgaris ist derzeit noch unbekannt (6;7).
Die Sicherheit und Wirksamkeit von Sarecyclin (1,5 mg/kg Körpergewicht, einmal täglich) wurden in zwei zwölfwöchigen multizentrischen, randomisierten, doppelblinden und placebokontrollierten Studien untersucht (SC1401, NCT02320149 und SC1402, NCT02322866), die insgesamt 2002 Probanden im Alter von neun Jahren und älter einschlossen. Im Vergleich zu Placebo zeigten sich statistisch signifikante Vorteile bezüglich der co-primären Wirksamkeitsendpunkte: die Verbesserung der globalen Bewertung des Hautbildes durch den Prüfer im Vergleich zum Ausgangswert und der absolute Rückgang der Anzahl entzündlicher Läsionen gegenüber dem Ausgangswert (8). Patienten, die beide Studien abgeschlossen haben (n = 483), wurden in eine offene Langzeitstudie (NCT02413346) zur Evaluation der Sicherheit von Sarecyclin aufgenommen (6). Sarecyclin zeigte eine gute Verträglichkeit in den Studien. Die Inzidenz von Nebenwirkungen (Treatment Emergent Adverse Events, TEAE) war unter Sarecyclin und Placebo vergleichbar und lag bei etwa 25–30 %. Die häufigsten TEAE (bei ≥ 2 % der Patienten in beiden Gruppen) waren Übelkeit (4,6 % Sarecyclin, 2,5 % Placebo), Nasopharyngitis (3,1 % und 1,7 %), Kopfschmerzen (2,7 % in beiden Gruppen) und Erbrechen (2,1 % und 1,4 %) in der Studie SC1401, und Nasopharyngitis (2,5 % Sarecyclin und 2,9 % Placebo) und Kopfschmerzen (2,9 % und 4,9 %) in der Studie SC1402. Vulvovaginale Candidose und vulvovaginale Mykosen traten nur unter Sarecyclin auf: 1,1 % bzw. 0,7 % in SC1401 und 0,3 % bzw. 1,0 % in SC1402.
Die US-Leitlinie empfiehlt Sarecyclin nur bedingt für die Behandlung von Akne auf der Grundlage der drei Studien mit hoher Ergebnissicherheit und auf der Grundlage von Diskussionen in der Arbeitsgruppe über den Zugang zur Behandlung und die Kosten. Sarecyclin wurde als sicher und gut verträglich eingestuft, mit geringer Inzidenz von gastrointestinalen Nebenwirkungen sowie Photosensibilität und Candida-Infektionen als Nebenwirkungen. Trotz des positiven Risiko-Nutzen-Verhältnisses wurde nur eine bedingte Empfehlung ausgesprochen aufgrund von Bedenken über die derzeit hohen Kosten der Behandlung, die den ungehinderten Zugang zur Aknebehandlung beeinträchtigen könnten. Die Kosten liegen derzeit bei 1120 USD pro 30-Tabletten-Packung (9). In Deutschland und in der EU ist Sarecyclin derzeit nicht verfügbar.
Clascoteron
Das topisch einzusetzende Clascoteron ist ein neuartiger Androgenrezeptor-Inhibitor, der aknegenetische Signalwege und die Talgproduktion hemmt und Entzündungsmediatoren reduzieren soll. Da er schnell in eine inaktive Form metabolisiert wird, dürfte die systemische Aktivität nach topischer Anwendung gering sein (10).
In zwei randomisierten, doppelblinden, klinischen Phase-III-Studien wurde die Wirksamkeit und Sicherheit von Clascoteroncreme 1 % im Vergleich zu einer wirkstofffreien Creme untersucht. Eingeschlossen wurden 1440 Männer und nicht schwangere Frauen im Alter von über neun Jahren mit mittelschwerer oder schwerer Akne, bei denen 30 bis 75 entzündliche Läsionen und 30 bis 100 nicht entzündliche Läsionen vorlagen. Die Behandlung erfolgte über zwölf Wochen zweimal täglich. Primäre Endpunkte waren der Anteil der Patienten mit einer Reduktion von mindestens zwei Punkten und ein Wert von 0 (klar) oder 1 (fast klar) in der globalen Einschätzung des Prüfers (Investigator’s Global assessment, IGA) und die Reduktion der nicht entzündlichen und entzündlichen Läsionen in Woche 12 gegenüber dem Ausgangswert (11).
In Woche 12 betrugen die Erfolgsraten in beiden Studien unter Clascoteron 18,4 % (Punktschätzung 2,3; 95 % Konfidenzintervall [CI] 1,4–3,8; p < 0,001) und 20,3 % (Punktschätzung 3,7; 95 % CI 2,2–6,3; p < 0,001) gegenüber 9,0 % bzw. 6,5 % unter der Behandlung mit wirkstofffreier Creme. Die Behandlung mit einprozentiger Clascoteroncreme führte in beiden Studien zu einer statistisch signifikanten Verringerung sowohl der nichtentzündlichen Läsionen als auch der entzündlichen Läsionen im Vergleich zur Behandlung mit wirkstofffreier Creme. Die meisten in beiden Studien aufgetretenen unerwünschten Ereignisse waren nicht schwerwiegend. Die häufigsten unerwünschten Ereignisse in den Studien waren Nasopharyngitis, Kopfschmerzen und oropharyngeale Schmerzen. Häufige unerwünschte Ereignisse unter Clascoteron, die als therapiebedingt eingestuft wurden, waren Schmerzen, Trockenheit, Erytheme, Hypertrichose und Hypersensitivität an der Applikationsstelle, Akne, Kontaktdermatitis, oropharyngeale Schmerzen (ursächlich nicht näher erklärt), Augenirritationen, Kopfschmerzen, Änderung der Haarfarbe und Peritonsillarabszess. 17 Patienten brachen die Studien vorzeitig ab, 12 unter der wirkstofffreien Creme und 5 unter Clascoteron aufgrund von nicht schweren Nebenwirkungen: Überempfindlichkeit an der Applikationsstelle, oropharyngeale Schmerzen, Talgdrüsenhyperplasie, akute Kontaktdermatitis im Gesicht und entpigmentierte Haare auf der Nase (jeweils n = 1). Die Clascoteron-Creme wurde 2020 in den USA zu Behandlung von Acne vulgaris bei Personen ab zwölf Jahren zugelassen (12). Als mögliche Nebenwirkungen sind vor allem lokale Reaktionen an der Applikationsstelle aufgeführt, aber auch Hyperkaliämie, polyzystische Ovarien und Amenorrhoe, wobei die letzten allerdings wohl eher als Ursache der Akne, denn als Nebenwirkung der topischen Therapie betrachtet werden könnten. In der EU soll eine Zulassung beantragt worden sein (13), mit der Vermarktung in Deutschland wird erst im Jahr 2025 gerechnet (14).
Die US-Leitlinie empfiehlt Clascoteron nur bedingt für die Behandlung von Akne. Die Empfehlung basiert auf den Ergebnissen der Zulassungsstudien und auf den Diskussionen der Arbeitsgruppe über den Zugang zur Behandlung und die Kosten. Auch hier bestehen Bedenken wegen der derzeit hohen Kosten der Clascoteron-Behandlung, die den ungehinderten Zugang zur Aknebehandlung beeinträchtigen könnten. Die 60-g-Packung kostet derzeit etwa 642 USD (9).
Literatur
- Eichenfield DZ, Sprague J, Eichenfield LF. Management of Acne Vulgaris: A Review. JAMA 2021; 326(20):2055–67. doi: 10.1001/jama.2021.17633.
- Reynolds RV et al. Guidelines of care for the management of acne vulgaris. J Am Acad Dermatol. 2024: S0190-9622(23)03389-3.
- Karoglan A, Gollnick HPM. Akne. Hautarzt 2021; 72(9):815–27. doi: 10.1007/s00105-021-04856-8.
- Nast A, Dréno B, Bettoli V, Bukvic Mokos Z, Degitz K, Dressler C et al. European evidence-based (S3) guideline for the treatment of acne – update 2016 – short version. J Eur Acad Dermatol Venereol 2016; 30(8):1261–8. doi: 10.1111/jdv.13776.
- Gebauer K. Acne in adolescents. Aust Fam Physician 2017; 46(12):892–5.
- Deeks ED. Sarecycline: First Global Approval. Drugs. 2019 Feb;79(3):325–9. doi: 10.1007/s40265-019-1053-4.
- FDA: Seysara®: Highlights of prescribing information. Stand: März 2023. Verfügbar unter: www.accessdata.fda.gov/drugsatfda_docs/label/2023/209521s015s016lbl.pdf.
- Moore A, Green LJ; Bruce S, Sadick N, Tschen E, Werschler P et al. Once-Daily Oral Sarecycline 1.5 mg/kg/day is Effective for Moderate to Severe Acne Vulgaris: Results from Two Identically Designed, Phase 3, Randomized, Double-Blind Clinical Trials. J Drugs Dermatol. 2018 Sep 1;17(9):987–996.
- Drugs.com. Drug Price Information [Stand: 26.8.2024]. Vwerfügbar unter: www.drugs.com/price-guide.
- Gerste RD. Acne vulgaris: Neuartiger topischer Androgenrezeptor-Hemmer reduziert Akne-Läsionen deutlich. Dtsch Arztebl 2020; 117(35-36): A-1622 / B-1387.
- Hebert A, Thiboutot D, Stein Gold L, Cartwright M, Gerloni M, Fragasso E, Mazzetti A. Efficacy and Safety of Topical Clascoterone Cream, 1%, for Treatment in Patients With Facial Acne: Two Phase 3 Randomized Clinical Trials. JAMA Dermatol. 2020 Jun 1;156(6):621–30. doi: 10.1001/jamadermatol.2020.0465.
- FDA: Winlevi®: Highlights of prescribing information. Stand: August 2020. Verfügbar unter: www.accessdata.fda.gov/drugsatfda_docs/label/2020/213433s000lbl.pdf.
- Pharmiweb.com. Cosmo announces submission of Winlevi® to the European Medicines Agency (EMA). Richmond, 10.10.2023. Verfügbar unter: www.pharmiweb.com/press-release/2023-10-10/cosmo-announces-submission-of-winlevi-to-the-european-medicines-agency-ema.
- Cosmo Pharmaceuticals N.V. Cosmo and Infectopharm Announce Signing of License and Distribution Agreement for Winlevi® in Germany, Italy and Austria. Dublin, 4.10.2022. Verfügbar unter: www.cosmopharma.com/news/cosmo-and-infectopharm-announce-signing-of-license-and-distribution-agreement-for-winlevi-in-germany-italy-and-austria.
Interessenkonflikte
Der Autor und die Autorin geben an, keine Interessenkonflikte zu haben.